
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示。要求同学们进行探究:确认这瓶溶液究竟是什么溶液?

【提出猜想】王老师提示:这瓶无色溶液只能是下列四种溶液中的一种:①硫酸镁溶液;②硫酸钠溶液;③硫酸溶液;④硫酸铵溶液
【查阅资料】
①常温下,相关物质的溶解度如下:
|
物质 |
MgSO4 |
Na2SO4 |
(NH4)2SO4 |
H2SO4 |
|
溶解度 |
35.1g |
19.5g |
75.4g |
与水任意比互溶 |
②(NH4)2SO4的水溶液显酸性
(1)【实.验探究】小明对王老师的提示进行了评价不可能是Na2SO4,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
|
实验操作 |
实验现象 |
实验结论 |
|
①取该溶液少许于试管中,向其中滴加几滴 溶液 |
溶液中有白色沉淀生成 |
猜想①成立 |
|
②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟标准比色卡对照 |
溶液pH小于7 |
猜想③成立 |
小雅对小明实验操作②的结论评价是 ,理由是 _;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
|
实验操作 |
实验现象 |
实验结论 |
|
取该溶液少许于试管中, ① ②将湿润的红色石蕊试纸放在试管口 |
①产生有刺激性气味的气体 ② |
猜想④成立,该反应的化学方程式为
|
(1)常温下Na2SO4溶液的溶质质量分数不可能达到20%。
(2)① NaOH (或氢氧化钠)(答案合理即可) 结论不正确(或结论错误) (NH4)2SO4溶液也呈酸性
(3)
|
实验操作 |
实验现象 |
实验结论 |
|
向试管中加入少量NaOH溶液并加热,将湿润的红色石蕊试纸放在试管口 |
有刺激性气味的气体产生, 红色石蕊试纸变蓝 |
(NH4)2SO4+2NaOH
|
【解析】
试题分析:从资料信息可以看出,硫酸钠的溶液解度是19.5g,在硫酸钠形成饱和溶液时,所得到的溶质质量分数最大只能是: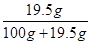 ×100%=16.3%,而达不到20%,所以小明认为药品不可能是硫酸钠溶液;能与硫酸镁反应产生白色沉淀的物质是氢氧化钠溶液,所以要证明该药品是硫酸镁,并产生白色沉淀现象,所加药品应该是氢氧化钠溶液;因为硫酸溶液、硫酸铵溶液都显酸性,其pH都小于7,所以小雅认为小明的实验操作②的结论是错误的;硫酸铵是铵态氮肥,它能与碱性物质反应并施放出氨气,氨气的水溶液就是氨水,显碱性,能使红色石蕊试纸变蓝色。
×100%=16.3%,而达不到20%,所以小明认为药品不可能是硫酸钠溶液;能与硫酸镁反应产生白色沉淀的物质是氢氧化钠溶液,所以要证明该药品是硫酸镁,并产生白色沉淀现象,所加药品应该是氢氧化钠溶液;因为硫酸溶液、硫酸铵溶液都显酸性,其pH都小于7,所以小雅认为小明的实验操作②的结论是错误的;硫酸铵是铵态氮肥,它能与碱性物质反应并施放出氨气,氨气的水溶液就是氨水,显碱性,能使红色石蕊试纸变蓝色。
考点:饱和溶液、盐的化学性质。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
 一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液导电是什么溶液?
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液导电是什么溶液?| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 |
溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸水,并跟比色卡对照 | 溶液pH小于7 |
猜想③成立 |
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中, |
猜想④成立,该反应的化学方程式为 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2013?齐河县一模)一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?
(2013?齐河县一模)一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 NaOH(或氢氧化钠)(答案合理即可) NaOH(或氢氧化钠)(答案合理即可) 溶液 |
溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟标准比色卡对照 | 溶液pH小于7 |
猜想③成立 |
| 实验操作 | 实验现象 | 实验结论 | ||||||||
| 取该溶液少许于试管中, 向试管中加入少量NaOH溶液并加热,将湿润的红色石蕊试纸放在试管口 向试管中加入少量NaOH溶液并加热,将湿润的红色石蕊试纸放在试管口 |
有刺激性气味的气体产生, 红色石蕊试纸变蓝 有刺激性气味的气体产生, 红色石蕊试纸变蓝 |
猜想④成立,该反应的化学方程式为 (NH4)2SO4+2NaOH
(NH4)2SO4+2NaOH
|
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 NaOH NaOH 溶液 |
溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟标准比色卡对照 | 溶液pH小于7 |
猜想③成立 |
| 实验操作 | 实验现象 | 实验结论 | ||||||||
| 取该溶液少许于试管中, 向试管中加入少量NaOH溶液并加热, 向试管中加入少量NaOH溶液并加热, 将湿润的红色石蕊试纸放在试管口 将湿润的红色石蕊试纸放在试管口 |
有刺激性气味的气体产生, 有刺激性气味的气体产生, 红色石蕊试纸变蓝 红色石蕊试纸变蓝 |
猜想④成立,该反应的化学方程式为 (NH4)2SO4+2NaOH (NH4)2SO4+2NaOH
|
查看答案和解析>>
科目:初中化学 来源: 题型:
 一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液是什么溶液?
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液是什么溶液?| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 NaOH NaOH 溶液 |
溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟比色卡对照 | 溶液pH小于7 | 猜想③成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水以任意比互溶 |
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 NaOH NaOH 溶液 |
溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,和比色卡对照 | 溶液的pH小于7 | 猜想③成立 |
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中, 加入少量的NaOH溶液,然后将湿润的红色石蕊试纸放在试管口 加入少量的NaOH溶液,然后将湿润的红色石蕊试纸放在试管口 |
有刺激性气味的气体产生,红色石蕊试纸变蓝 有刺激性气味的气体产生,红色石蕊试纸变蓝 |
猜想④成立,该反应的化学方程式 (NH4)2SO4+2NaOH= Na2SO4+2NH3↑+2H2O (NH4)2SO4+2NaOH= Na2SO4+2NH3↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com