
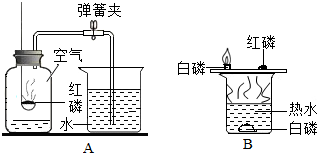
分析 (1)红磷在空气中燃烧生成五氧化二磷,氧气约占空气总体积的五分之一;
(2)可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可;
(3)灭火的方法有:移走可燃物,隔绝氧气,降低温度到可燃物的着火点以下.
解答 解:(1)A实验中红磷燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,实验说明氧气的体积约占空气的五分之一,该实验成功的关键是装置气密性好,实验前夹紧止水夹,红磷过量或足量,冷却到室温后才打开止水夹.
故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,五分之一,①②③④.
(2)B实验中,由铜片上白磷燃烧而热水中的白磷没有燃烧的现象可以得知,可燃物燃烧的条件之一是与氧气接触.
故填:可燃物与氧气接触.
(3)实验时,不慎将酒精洒到桌面并着火,可用湿布覆盖,其灭火原理是隔绝氧气,降低可燃物的温度.
故填:隔绝氧气,降低可燃物的温度.
点评 教室内的空气不新鲜,不能用于测定空气中氧气含量的实验,要注意理解.


科目:初中化学 来源: 题型:选择题
| A. | 核外电子数 | B. | 核电荷数 | C. | 相对原子质量 | D. | 原子所带的电性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
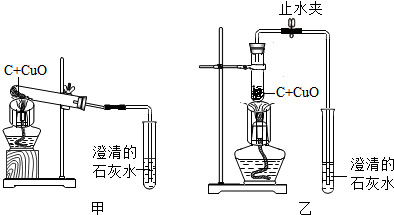
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
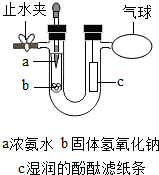 某同学在学完《分子和原子》后,对教材中的实验进行了如图改进:
某同学在学完《分子和原子》后,对教材中的实验进行了如图改进:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
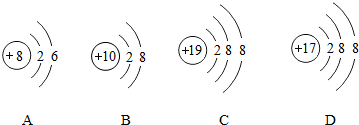
| A. | 它们表示的是同一种元素 | |
| B. | 它们的核外电子数相同 | |
| C. | 它们都具有相对稳定的结构 | |
| D. | 它们依次表示原子、原子、阳离子、阴离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.燃烧条件 | B.认识粒子 |
| ①可燃物 ②氧气(或空气) ③温度达到着火点 | ①原子比分子小 ②分子运动原子不运动 ③分子由原子构成 |
| C.化学元素 | D.化学之最 |
| ①缺铁可能导致贫血 ②缺钙可能导致弱智 ③缺碘可能导致佝偻病 | ①熔点最低的金属是汞 ②地壳中含量最多的元素是氧 ③导电性最好的金属是铜 |
| A. | 燃烧条件 | B. | 认识粒子 | C. | 化学元素 | D. | 化学之最 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 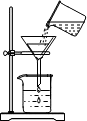 过滤 | B. | 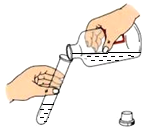 倾倒液体 | C. | 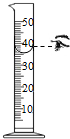 量取35毫升液体 量取35毫升液体 | D. | 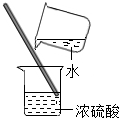 稀释浓硫酸 稀释浓硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管底部有黑色固体 | 燃烧产物中肯定有C |
| (2) | 取少量(1)所得上层溶液,加入过量的BaCl2溶液 | 有白色沉淀生成 | 燃烧产物中肯定有Na2CO3 |
| (3) | 取少量(2)所得上层清液,加入CuSO4(或CuCl2)溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有Na2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学兴趣小组用如图燃烧红磷的方式做空气中氧气体积成分测定实验时,发现进入集气瓶内的水超过了$\frac{1}{5}$.全组人员为此纳闷,请问你能帮他们找出原因:燃烧匙伸入集气瓶时太慢、红磷燃烧时没有夹紧止水夹(至少找两点).
某化学兴趣小组用如图燃烧红磷的方式做空气中氧气体积成分测定实验时,发现进入集气瓶内的水超过了$\frac{1}{5}$.全组人员为此纳闷,请问你能帮他们找出原因:燃烧匙伸入集气瓶时太慢、红磷燃烧时没有夹紧止水夹(至少找两点).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com