
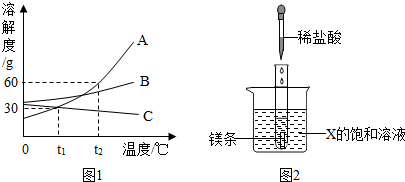
分析 (1)根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
(2)根据不饱和溶液转变成饱和溶液的方法解答;
(3)饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
(4)盐酸与镁条反应放热,烧杯中出现浑浊,说明温度升高,溶解度变小,因此X是C物质.
解答 解:(1)t1℃时,A物质的溶解度是30g,将30gA物质加入到50g水中充分溶解,只有15g溶解在水中,所形成溶液的质量为65g.t2℃时,A、B、C三种物质中,溶解度最大的是A>B>C.
(2)B物质的溶解度随温度的升高而增大,t2℃时,将B物质的不饱和溶液转变成饱和溶液可采取降低温度或加入B物质;
(3)将t2℃的A、B、C三种物质的饱和溶液中,A溶液的质量分数最大,C溶液的质量分数最小,降温至t1℃时,所得溶液中溶质质量分数最小的仍然是C溶液,因为A和B在t1℃时的溶解度都大于C在t2℃的溶解度.t1℃时溶液中溶质的质量分数由大到小的顺序是B>A>C;
(4)盐酸与镁条反应放热,烧杯中出现浑浊,说明温度升高,溶解度变小,因此X是C物质,故答案为:C.
答案:
(1)65;A;
(1)降低温度或加入B物质;
(3)B>A>C;
(4)C.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:初中化学 来源: 题型:解答题
 海水中蕴含着80多中元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氯气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.
海水中蕴含着80多中元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氯气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②④⑤ | C. | ①③⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| O2- | OH- | CO32- | Cl- | SO42- | NO3- | |
| M2+ | 难溶 | 难溶 | 难溶 | 易溶 | 易溶 | 易溶 |
| A. | ①②④⑦ | B. | ⑤⑥⑦⑧ | C. | ②④⑥ | D. | ①③⑤⑧ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | N2 | B. | NO2 | C. | NO | D. | N2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com