
【题目】下列有关物质燃烧现象的叙述中,正确的是
A.铁丝在氧气中燃烧:火星四射,生成红色固体
B.硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体
C.镁条在空气中燃烧:发出耀眼的白光,只生成一种黑色固体
D.红磷在空气中燃烧:发出白光,生成大量的白色烟雾
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:初中化学 来源: 题型:
【题目】硒是人体必需的一种微量元素,严重缺硒有可能诱发皮肤疾病.已知硒的原子序数为34,质子数与中子数之和为79.下列有关硒原子的说法中,不正确的是
A.核电荷数为79
B.核外电子数为34
C.质子数为34
D.中子数为45
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)氯化钠是重要的调味品,是舌尖上最不可缺少的味道。下面三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。

(1)图1是金属钠与氯气反应生成氯化钠的微观示意图,氯化钠由 构成(填微粒符号)。由图1可知,元素的化学性质与原子结构中的 (填字母序号)有密切的关系;
A.最外层电子数 B.内层电子数 C.质子数
(2)图2描述了NaOH溶液与盐酸反应的微观实质,图中A、B、C处应填入的化学符号依次为 ;
(3)图3所示的四种物质中属于氧化物的是 (填化学式),请标出NaClO2中氯元素的化合价 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)纳米碳酸钡是一种重要的化工产品,下图是某厂生产纳米碳酸钡的工艺流程。请回答下列问题:

(1)碳酸钡的碳元素的化合价为 。
(2)试剂A的化学式为 ,操作1、操作2的名称是 ,若在实验室中进行该操作,实验中的玻璃棒的作用是 。
(3)写出纳米碳酸钡与稀盐酸发生反应的化学方程式: 。
(4)该流程操作2得到的滤液中含有KCl,其用途是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)化学兴趣小组同学将铝丝插入硫酸铜溶液中时,发现生成红色固体物质的同时有较多的气泡放出。生成了什么气体?同学们决定进行探究。
【提出猜想】放出的气体可能是SO2、O2、H2的一种或几种,提出猜想的依据是 。
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是_____________________________________。经检验不是O2。
(2)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。

【实验探究】实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;这样操作的目的是 。
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色。
结论:铝丝与硫酸铜溶液反应时,产生的气体是_________________。该气体与氧化铜的反应的化学方程式为 。
【思维拓展】由上述实验可以推出,硫酸铜溶液中可能含有____________。
注意:答对(3)(4)奖励4分,但化学试卷总分不超过60分。
(3)丙同学用砂纸将截下的一段铝丝长时间用力反复打磨,然后将打磨后的铝丝放入硫酸铜溶液中,在横截面处现象明显,但在铝丝表面无明显现象,请问可能的原因是
(4)丁同学用试管取2ml硫酸铜溶液,向试管中滴加氢氧化钠溶液,刚开始并未发现预料中的蓝色沉淀现象,其原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)氢化钙固体是登山运动员常用的能源提供剂。探究小组在烧杯中放入10g氢化钙样品,再加入到20g水充分搅拌,完全反应后测得烧杯内物质的总质量为29.2g。(已知氢化钙(CaH2)与水反应的化学方程式为:CaH2 + 2H2O ![]() Ca(OH)2 +2 H2↑)
Ca(OH)2 +2 H2↑)
请计算:
(1)生成氢气的质量。
(2)样品中氢化钙的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)我国著名化学家侯德榜发明的“联合制碱法”主要原理是:I.向浓氨水中通入足量的CO2,使氨气、水和CO2发生化合反应而生成NH4HCO3溶液;II.向所得溶液中加入食盐细粒,充分搅拌,会析出溶解度较小的小苏打固体并得到化肥溶液;III.加热析出的固体制取纯碱。此法经过调整并应用于化工产业,某化工企业的工艺流程示意图如下:

请完成下列填空:
(1)“联合制碱原理II”中发生反应的化学方程式为 。
(2)在如图的流程中,先加Ca(OH)2溶液的目的是 ,再加入Na2CO3溶液的目的是 。
(3)“操作1”的名称是 ,“氨化溶液”后,溶液的pH 7(填:“大于”、“小于”或“等于”),从而有利于吸收“气体A”,气体A为 (填名称)。
(4)利用“270℃以上小苏打完全分解,纯碱受热不分解”的性质,化学兴趣小组的同学对实验室所购纯碱(假设所含杂质均为小苏打)进行了如下实验:称取20.00g干燥的固体样品放入坩埚,300℃恒温加热至质量不变,在干燥器中冷却后称量残留固体质量为19.38g。
根据题目所给信息,计算该样品中纯碱的质量分数(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(15分)碳酸钠、碳酸氢钠是中学常见的化合物。
探究一:碳酸钠、碳酸氢钠与酸反应
如图所示,将两气球内的NaHCO3和Na2CO3同时倒入试管中。已知盐酸足量,且装置气密性良好。
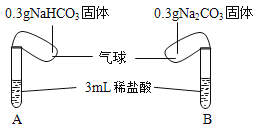
回答下列问题:
(1)碳酸钠俗名是 。
(2)实验过程中观察到的现象是: 。
(3)NaHCO3和Na2CO3都能与盐酸反应产生二氧化碳、水和氯化钠。任写出其中一个反应的化学方程式 。
(4)已知NaHCO3、Na2CO3的相对分子质量分别为84、106,通过计算:实验结束后, (填“A”或“B”)试管的气球更大。
探究二:碳酸氢钠、碳酸钠固体与酸反应的热效应
【发现问题】在探究一实验过程中用手触摸试管,发现盛NaHCO3的试管温度降低,而盛Na2CO3的试管温度升高。
【猜想与推测】甲同学由此推测:NaHCO3和盐酸反应为吸热反应,Na2CO3和盐酸反应为放热反应。
【实验与数据】乙同学认为甲同学推测不妥,通过以下多次实验后取平均值数据记录如下:
步骤① | 步骤② | 步骤③ | 步骤④ | 步骤⑤ |
测量10mL水温/℃ | 加入物质0.5 g | 溶解后测量溶液温度t1/℃ | 静置一段时间后测量溶液温度t2/℃ | 加入20%盐酸10 mL反应后测量溶液温度t3/℃ |
20 | NaHCO3 | 18.5 | 20.0 | 20.8 |
20 | Na2CO3 | 23.3 | 20.0 | 23.7 |
【分析与结论】
(1)由步骤①~③比较得到的结论是 。
(2)由步骤④~⑤比较得到的结论是: 。
(3)结合上面探究活动,你认为甲同学推测的不妥之处是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com