

分析 (1)从分液漏斗中加入的是液体,所以加入的是过氧化氢溶液,锥形瓶中加入的是固体,是二氧化锰;过氧化氢溶液在二氧化锰催化作用下生成水和氧气去分析解答;
(2)(3)(4)利用排水法收集 的气体比排空气法收集的气体纯净,并结合氧气的密度和溶解性分析解答;
(5)反应物接触越充分、浓度越大、温度越高,反应速率越快.
解答 解:(1)分液漏斗中加入的是液体,所以加入的是过氧化氢溶液,锥形瓶中加入的是固体,是二氧化锰;过氧化氢溶液在二氧化锰催化作用下生成水和氧气,故化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)氧气不易溶于水且密度比空气大,所以可用排水法或向上排空气法收集,利用排水法收集的气体比排空气法收集的气体纯净,甲收集的氧气比乙纯说明甲用的是排水法,乙用的是向上排空气法收集;
(3)甲同学选择D装置收集氧气的依据是氧气不易溶于水;当集气瓶口有大气泡逸出时说明集气瓶已满;
(4)乙同学选用B收集装置的依据是氧气的密度比空气大;证明氧气已集满的方法是把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了;
(5)A、装置A中反应剧烈,产生大量的氧气,可能会引起爆炸,为了控制反应,可通过控制液体的滴加速度达到控制二者的接触的目的;故A正确;
B、用体积小的锥形瓶,会因产生大量的氧气散发不出去引起爆炸;故B错误;
C、加热反应物会使反应更加剧烈,更加不易控制,故C错误;
故答案为:
(1)过氧化氢溶液 二氧化锰 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)D、B;
(3)氧气不易溶于水;
(4)氧气的密度比空气大
(5)A
点评 本题主要考查了实验室制取氧气的发生和收集装置的选取,选择发生装置通常考虑反应物的状态和反应条件,选择气体的收集方法通常依据气体的密度和溶解性,考查学生分析、解决问题的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
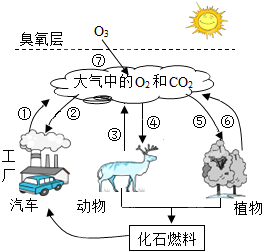 如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图,回答下列问题:
如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是用比例模型来表示物质间发生化学变化的微观示意图,图中“●”、“○”分别表示两个不同元素的原子,能用该图示表示的化学反应是( )
如图是用比例模型来表示物质间发生化学变化的微观示意图,图中“●”、“○”分别表示两个不同元素的原子,能用该图示表示的化学反应是( )| A. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | B. | N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 | ||
| C. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | D. | N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com