
【题目】化学在日常生活中有广泛应用
(1)根据如图衣服标签的部分说明回答下列问题:

①面料中的棉属于_______(填“天然”或“合成”,下同)有机高分子材料,面料中的涤纶属于________有机高分子材料,
②你知道聚酯纤维有下列哪三个优点____________(填序号)
A. 强度高、弹性好 B. 耐磨
C. 吸水性、透气性好 D. 耐化学腐蚀
(2)均衡的膳食结构可以保障身体健康。某种食品的配料标签如图所示:
该配料中富含蛋白质的物质是____________。从营养均衡的角度看,该食品中除水外,还缺少的营养素是____________。
(3)以下是我们日常生活中常用的清洗剂,其名称及有效成分如下表:
生活中的 用品 |
|
活氧彩漂 |
污渍爆炸盐 |
有效成分 | 盐酸 | 过氧化氢 | 过碳酸钠 |
①清除以下物质,可以使用洁厕灵的是____________(填字母序号)。
A. 铁锈 B. 水垢(主要成分为碳酸钙和氢氧化镁) C. 油渍
②“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是____________(填序号)。
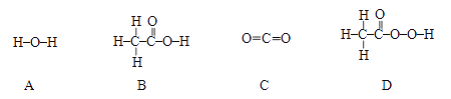
【答案】 天然 合成 ABD 鸡蛋 维生素 AB D
【解析】本题考查有机高分子材料的分类,营养素的来源和合理饮食,酸的化学性质。
(1)①面料中的棉属于天然有机高分子材料、面料中的涤纶属于合成有机高分子材料;②强度高、弹性好,耐磨、耐化学腐蚀都是合成纤维的优点。合成纤维的吸水性、透气性都稍差,故选ABD;
(2)鸡蛋中富含蛋白质,小麦粉、白砂糖富含糖类、食盐富含无机盐、棕榈油富含油脂,从营养均衡的角度看,该食品中除水外,还有维生素;
(3)①洁厕灵有效的成分是盐酸,可以和铁锈反应生成溶于水的物质,将铁锈除去,可以和水垢反应生成易溶于水的物质,将水垢除去,但不能和油污反应,不能除去油污,故选AB;
②根据分子结构可以看出,D中含有过氧基,能用于漂洗衣物、杀菌消毒,故选D;


科目:初中化学 来源: 题型:
【题目】如图所示A、B两种固体物质的溶解度曲线:
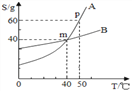
(1)当温度为______℃时,A物质与B物质的溶解度相等。
(2)50℃时,20g水中加入____g A物质,恰好得到饱和溶液。
(3)40℃时,如果A、B两种溶液的质量分数相等,该质量分数可以是_________(填编号)。
A.20% B.28% C.40% D.50%
(4)除去固体B中混有的少量固体A,具体的操作流程是________(填序号)。
①蒸发结晶 ②洗涤干燥 ③加水溶解 ④趁热过滤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生活生产中有着非常广泛的应用。
(1)生铁和钢都是铁的合金,从组成上看,二者性能不同的原因是_____。
(2)下列物品所使用的主要材料属于金属材料的是_____。
A.玻璃钢花盆 B.不锈钢炊具 C.橡胶手套 D.羊毛围巾
(3)有些金属元素是人体的营养元素,下列金属元素属于人体常量元素的是_____。
A.钠 B.铁 C.钙 D.锌
(4)用下图装置完成 CO 还原 Fe2O3 的实验。缓慢通入一定量的 CO。点燃酒精喷灯,继续 通入 CO。一段时间后,当粉末全部变为黑色时,停止通入 CO,熄灭酒精喷灯。
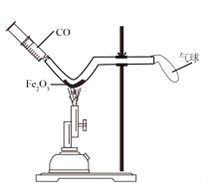
①CO 与 Fe2O3 反应的化学方程式是_____。
②在冷却过程中,为防止管中黑色粉末表面因与空气接触而变为红色,应补充的操作 是_____。
③将黑色固体中加入 CuSO4 溶液,发生反应的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料包括纯金属以及它们的合金。
(1)铁锅、铝锅和铜火锅可以用来炒菜、做饭和涮肉,是因为铁、铝、铜能够________。
(2)为了验证铁、铝、铜的金属活动性顺序,某同学选择了打磨过的铁丝,他还需要选择的两种盐溶液是__________________。写出实验中发生反应的化学方程式:_____________________。
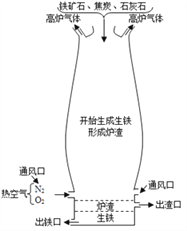
(3)炼铁的原理是利用一氧化碳与氧化铁的反应,化学方程式为______________________,该反应中氧化铁表现出______________(填“氧化性”或“还原性”)。如图是炼铁高炉示意图,写出原料焦炭的一个作用:_________________________。
(4)5g某钢样在纯氧中完全燃烧,得到0.33g二氧化碳。求此钢样中碳的质量分数______。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三物质的溶解度曲线,下列分析不正确的是
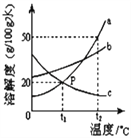
A. t2 ℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B. t2 ℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C. 将c的饱和溶液变为不饱和溶液,可采用升温的方法
D. 将t2 ℃时a、b、c三种物质的饱和溶液降温至t1 ℃时,所得溶液的溶质质量分数关系是:b>a﹦c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活、生产关系密切。请回答下列问题:
(1)下图为某抗酸药的实物图,该图标示的物质中,含有的金属元素是__________(写出一种塑即可),属于有机合成材料的是__________。
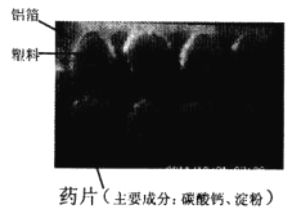
(2)淀粉属于__________(填字母序号)。
A.维生素 B蛋白质 C.油脂 D.糖类
(3)某种抗酸药的主要成分是三硅酸镁Mg2Si3O8·nH2O),能与盐酸发生复分解反应,那么,反应后产物中含镁的化合物是____________________(填化学式)。
(4)生产加碘盐通常是在食盐中加入碘酸钾(KIO3),碘酸钾中碘元素的化合价为__________价。
(5)沾染了油污的衣物用洗洁精就可以洗净,这是利用了洗洁精的_________________作用。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据图所示实验回答问题。
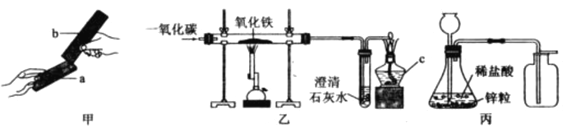
(1)甲实验中金属片a、b分别是纯铜片和黄铜片的一种,相互刻画后,只有a上留下划痕,则金属片b是__________(选填“纯铜片”或“黄铜片”)。
(2)乙实验中仪器c的名称是__________,在通入一氧化碳前应先进行__________操作,以确保实验安全。
(3)丙是实验室制取氢气的装置,有关反应的化学方程式为____________________。图中有一处错误,请指出______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验是实现科学探究的重要途径。请回答以下有关化学实验的问题。
(1)如图是实验室制取气体的装置图:
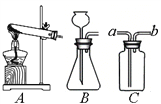
①A中的试管口为什么应略向下倾斜?_________________
②写出选用B制取氧气的化学方程式。__________________
③如果利用C装置,收集某气体,气体从a端通入,如何检验该气体?____________
(2)如图是某同学设计的趣味实验装置,其气密性良好。
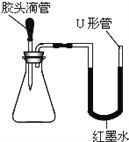
①若锥形瓶中充满CO2,胶头滴管中的物质是饱和的澄清石灰水,则挤压胶头滴管后能观察到什么现象?________________________
②若将胶头滴管中的物质滴入锥形瓶后,能明显观察到U形管中红墨水的液面左低右高,甚至从右端溢出。请推测胶头滴管和锥形瓶中的物质,并按反应类型的要求将化学方程式写在下边。
化合反应___________________;复分解反应______________________ 。
(3)实验室制氧气时将0.8g二氧化锰与一定量氯酸钾共热到质量不减少为止,称得残渣质量为15.7g。求:原氯酸钾的质量是多少g_____________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习和理解化学知识。请你一起研究学习,并回答有关问题。

研究问题:水溶液中复分解反应的实质
相关信息:(Ⅰ)电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小。
(Ⅱ)相同温度下同种溶液电导率越大,离子浓度越大。
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示。
①写出Ba(OH)2与H2SO4反应的化学方程式________________________。
②M点时电导率为零,离子浓度也几乎为零,此时混合液体静置后呈______色;
③通过对甲曲线的分析,下列说法错误的是_____(填序号)。
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
B.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示。
①通过对乙曲线的分析,下列说法正确的是________(填序号)。
A.实际参加反应的是Ba2+和SO42﹣结合成了BaSO4,Na+和OH﹣还是以离子形式存在于溶液中
B.溶液红色只会变浅,但不会褪去
②N点时,溶液中大量含有的离子是__________________(填离子符号,至少写两种)。
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度_______(填“增大”或“减小”)。
(注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分。)
(3)拓展:①请根据示例仿写离子方程式。示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式:________________________________。
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失。请推测此过程的溶液中Ca2+的浓度变化情况_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com