
| 实验内容 | 实验操作及现象、结论 | 化学方程式 |
| 用稀硫酸除铁锈 | 铁锈逐渐 溶解 溶解 ,溶液呈黄 黄 色. |
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O Fe2O3+3H2SO4═Fe2(SO4)3+3H2O |
| 鉴别熟石灰和石灰石 | 滴入 稀盐酸 稀盐酸 溶液,有气泡 气泡 产生的是石灰石. |
Ca(OH)2+2HCl═CaCl2+2H2O ;CaCO3+2HCl=CaCl2+H2O+CO2↑ Ca(OH)2+2HCl═CaCl2+2H2O ;CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 实验内容 | 实验操作及现象、结论 | 化学方程式 |
| 用稀硫酸除铁锈 | 铁锈逐渐 溶解,溶液呈黄 色. | Fe2O3+3H2SO4═Fe2(SO4)3+3H2O |
| 鉴别熟石灰和石灰石 | 滴入稀盐酸 溶液,有气泡 产生的是石灰石 | Ca(OH)2+2HCl═CaCl2+2H2O ;CaCO3+2HCl=CaCl2+H2O+CO2↑ |


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品适量于试管或烧杯中,加水溶解,再滴加几滴酚酞试剂 | 溶液变红 溶液变红 |
样品中有氢氧化钙存在 |
取样品适量于试管或烧杯中,向样品中滴加稀盐酸 取样品适量于试管或烧杯中,向样品中滴加稀盐酸 |
有气泡产生 有气泡产生 |
样品中有碳酸钙存在 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 点燃蜡烛,将一根火柴横放在火焰上方片刻 | 火柴梗 两端 两端 最先烧焦(填“两端”或“中间”) |
蜡烛火焰的 外焰 外焰 温度最高 |
| 将一个干冷的烧杯罩在火焰上方 | 烧杯内壁出现 水雾 水雾 |
蜡烛燃烧生成 水 水 |
| 将一个内壁蘸有澄清石灰水的烧杯罩在火焰上方 | 石灰水变 浑浊 浑浊 |
蜡烛燃烧生成 二氧化碳 二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
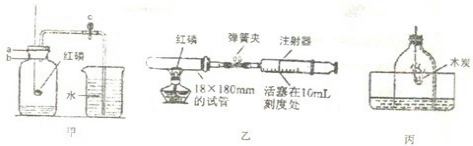
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com