
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:阅读理解
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2(2 Na2CO3?3 H2O2 )=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解;Ⅰ、制备研究:如图1是制备过碳酸钠的工艺流程.  请回答问题: (1)反应器中发生反应的化学方程式为 2Na2CO3+3H2O2═2Na2CO3?3H2O2 2Na2CO3+3H2O2═2Na2CO3?3H2O2 ;(2)生产中,反应及干燥均需在较低温度下进行,原因是 防止过碳酸钠分解,影响产量和产率 防止过碳酸钠分解,影响产量和产率 ;(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为 过碳酸钠在NaCl溶液中溶解度较小,易析出晶体 过碳酸钠在NaCl溶液中溶解度较小,易析出晶体 .(4)操作A的名称是 过滤 过滤 ,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒 玻璃棒 和漏斗 漏斗 ;(5)洗涤过碳酸钠晶体最好选用 B B .A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液 (6)母液可以循环使用,其中主要含有的溶质是 NaCl NaCl 和Na2CO3(或H2O2) Na2CO3(或H2O2) ;Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数. 小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验. [实验步骤]:① 检查气密性 检查气密性 ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中不再产生气体 不再产生气体 时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.[实验分析及数据处理]: (7)完善实验步骤的相关内容:① 检查气密性 检查气密性 、④不再产生气体 不再产生气体 ;(8)实验中,水的作用是 溶解过碳酸钠,利于其分解 溶解过碳酸钠,利于其分解 ;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是MnO2(或CuO) MnO2(或CuO) (填化学式);(9)实验中, A A ,则开始收集气体;A.刚开始出现气泡时 B.当气泡均匀连续出现时 C.若用带火星木条放在导管口部,复燃时 (10)若量筒中收集到气体的体积是224mL(通常情况下,氧气的密度近似为1.43g?L-1.),计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr(2Na2CO3?3H2O2)=314、Mr(O2)=32] 95% 95% ;[实验反思]: (11)经过讨论,小组同学一致认为测定结果偏大,可能原因是 滴入的水占据了锥形瓶内的体积,使得O2体积偏大 滴入的水占据了锥形瓶内的体积,使得O2体积偏大 ;(12)量筒中长导管的作用是 起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸) 起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸) ;(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由. 不正确,装置中原有空气和生成的O2等体积代换 不正确,装置中原有空气和生成的O2等体积代换 ;(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为 93.6% 93.6% .(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数? 想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定 想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定 .(只需给出简要的方案)
查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 金属材料在国防建设中起着重要的作用,如图1为歼-15飞机在辽宁舰上起飞.  (1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 硬度大、密度小 硬度大、密度小 .(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 氧气与水蒸气 氧气与水蒸气 共同作用的结果.铁锈的成分主要是Fe2O3?xH2O Fe2O3?xH2O (填化学式).(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属.小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验: ①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 所用酸的种类不同 所用酸的种类不同 .②实验二中,若出现 铁丝表面附着红色固体 铁丝表面附着红色固体 现象,可证明铁的活动性强于铜,该反应的化学方程式为Fe+CuSO4=FeSO4+Cu Fe+CuSO4=FeSO4+Cu .(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,CO2被充分吸收,氧化铁反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为Wg). ①装置A中生成铁的化学方程式为 3CO+Fe2O3
3CO+Fe2O3 ,装置C的作用是
将CO燃烧防止其污染空气 将CO燃烧防止其污染空气 .②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是 装置A在反应前后的质量变化 装置A在反应前后的质量变化 或装置B在反应前后的质量变化 装置B在反应前后的质量变化 .③设计实验证明锌、铁、铜三种金属的金属活动性强弱,要求写出实验步骤、现象和结论.
查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 (2013?江阴市一模)某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究. (一)【定性探究】 [查阅资料]
(1)探究两者水溶液酸碱性的差异 小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变 红 红 色,但食用纯碱溶液中颜色更深,由此推测可能食用纯碱 食用纯碱 溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用pH试纸 pH试纸 进行测定.(2)验证两种粉末的稳定性 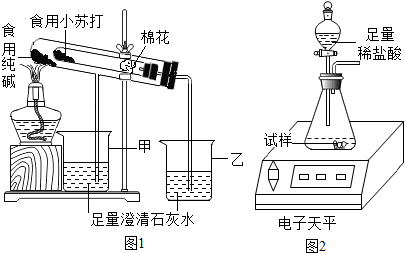 在老师的指导下,该小组按图1装置进行实验操作,观察到 乙 乙 (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为2NaHCO3
2NaHCO3 ,装置中棉花的作用是
防止加热时小苏打(或NaHCO3)粉末进入导管 防止加热时小苏打(或NaHCO3)粉末进入导管 .【拓展延伸】 (3)通过学习,我们知道小苏打(NaHCO3)除用于食品工业外,在日常生活及实验室中还有很多应用,试举一例: 治疗胃酸过多 治疗胃酸过多 .(二)【定量探究】 (4)取食用纯碱粉末试样,利用图2装置进行实验测定,数据记录如下:
4.4 4.4 g.②通过计算确定食用纯碱粉末中Na2CO3的质量分数为 96.4 96.4 %(结果保留一位小数)③如果测得的结果比实际纯度高,可能的原因是 稀盐酸挥发出的HCl气体(或水蒸气)随CO2气体排出而导致所测纯度偏大 稀盐酸挥发出的HCl气体(或水蒸气)随CO2气体排出而导致所测纯度偏大 .(答一种即可)查看答案和解析>> 科目:初中化学 来源: 题型: 2012年3月22日是第二十个“世界水日”.让我们一起来关注水,参与讨论下列有关问题: (1).下列有关水的知识,其中不正确的是 BC BC A.水是一种最常见的溶剂,自然界中的水大多数含有杂质 B.水中Ca2+、Mg2+的增多会引起水体的富营养化污染 C.用过滤或蒸馏的方法能降低水的硬度 D.在水溶液中发生化学反应,反应速度比较快而且充分 (2).干旱时期,人们被迫取浑浊的河水作生活用水,向所取的河水中加入明矾的作用是: 吸附杂质,使其沉降 吸附杂质,使其沉降 .为了除去水样中的颜色和异味,可向水中加入活性炭 活性炭 ,该过程属于物理 物理 (填“物理”或“化学”)变化.高铁酸钠(Na2FeO4)可用于饮用水消毒,其中铁元素的化合价是+6价 +6价 .有些人打井取用地下水,测定地下水的酸碱度可用pH试纸 pH试纸 .政府组织人工降雨活动,使用物质干冰的物理性质是固体 固体 (任写一种)(3).生活中变瘪的乒乓球放入热水中能鼓起来,请用分子的基本性质解释: 分子间间隔随温度升高而增大 分子间间隔随温度升高而增大 ,水是生命之源,但不提供能量,请举一食物能弥补水的不足,如:馒头 馒头 ,水的用途很广,请举出水在实验室中的一个用途水用于配制溶液 水用于配制溶液 .查看答案和解析>> 科目:初中化学 来源: 题型:解答题
|
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
| 称量项目 | 称量时间 | 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com