
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)双氧水缓慢分解生成水和氧气,反应的化学方程式为:2H2O2═2H2O+O2↑.
(2)CO2通入水中反应生成碳酸,反应的化学方程式为:CO2+H2O=H2CO3.
(3)纯碱与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(4)小苏打与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑.
(5)以生石灰(CaO)为脱硫剂,高温下与废气中的SO2与O2化合生成CaSO4,反应的化学方程式为:2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
故答案为:(1)2H2O2═2H2O+O2↑;(2)CO2+H2O=H2CO3;(3)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;(4)NaHCO3+HCl═NaCl+H2O+CO2↑;(5)2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.


科目:初中化学 来源: 题型:选择题
| A. | C | B. | SiO2 | C. | Si | D. | CO |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不慎碰倒酒精灯,酒精在桌面上燃烧起来,立即用水冲 | |
| B. | 炒菜时,锅里的油起火应立即端下油锅 | |
| C. | 厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| D. | 图书馆内图书起火,立即用泡沫灭火器扑灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
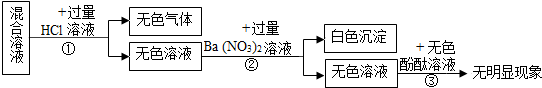
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
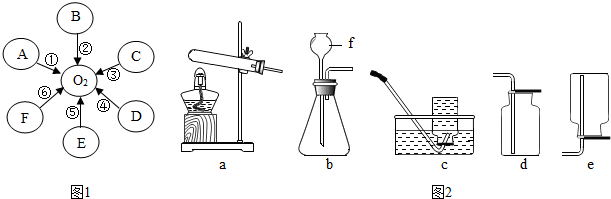
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
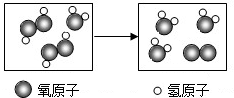
| A. | 反应前后分子个数不变 | |
| B. | 反应后的生成物都是氧化物 | |
| C. | 该反应是分解反应 | |
| D. | 反应的化学方程式为2H2O2+H2O═3H2O+O2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
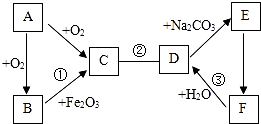 A~F是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“→”表示一种物质转化成另一种物质.部分生成物和反应条件已略去).A、B、C三种物质中都含有碳元素,A为黑色固体;D、E、F三种物质中都含有钙元素,F可作干燥剂.请回答下列问题:
A~F是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“→”表示一种物质转化成另一种物质.部分生成物和反应条件已略去).A、B、C三种物质中都含有碳元素,A为黑色固体;D、E、F三种物质中都含有钙元素,F可作干燥剂.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com