
根据化学式计算其中某种元素的相对原子质量及其中某种元素的化合价解此类问题必须掌握相对分子质量的概念及相对分子质量的计算方法和化学式的意义,才能正确求出某元素的相对原子质量和某元素的化合价,如:某化合物的化学式为HnAO2n-1,若化合物的相对分子质量为M,则元素A的化合价为________,元素A的相对原子质量为________.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:阅读理解

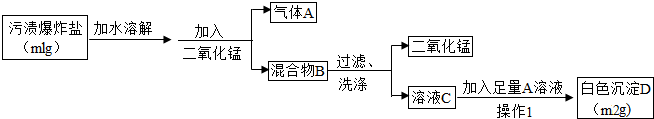
| ||
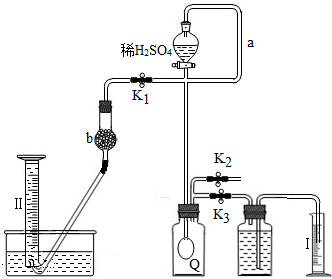
查看答案和解析>>
科目:初中化学 来源: 题型:
| 500g食品的味精含量/mg | |
| 春卷 | 400 |
| 排骨 | 240 |
| 水饺 | 130 |
查看答案和解析>>
科目:初中化学 来源:2010年广东省佛山市高中阶段学校招生考试化学试题 题型:038
2009年底武广高速铁路的开通,标志着我国铁路事业进入一个崭新的时代.铺设无缝钢轨.需要用大量的钢铁.钢铁在生活中应用非常广泛,认识铁的有关知识很有意义.结合所学知识,完成下题.
(1)铁有多种氧化物,根据下列信息推断它们的化学式∶
①某铁的氧化物中铁元素的化合价为+3价,氧元素的化合价为-2价,则该铁的氧化物的化学式为________________.
②某铁的氧化物化学式为FexOy,相对分子质量为72,则该铁的氧化物的化学式为________.
③某铁的氧化物可还原得到铁,化学方程式为________+4CO![]() 3Fe+4CO2,则“”中铁的氧化物的化学式为________________.
3Fe+4CO2,则“”中铁的氧化物的化学式为________________.
(2)为了分析生铁中铁的含量,某学习小组进行了实验研究,即取6 g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见下图).说明∶生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应.

①铁完全反应用去盐酸的质量为________g.
②生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
③某同学列出了如下计算式∶
生铁与盐酸刚好反应完全时所得溶液质量=(73+6-a)g
小明对该计算式提出了质疑,请指出其中的错误________________.
④小华另设计了一个实验方案,即用6 g生铁粉与20%的硫酸铜溶液反应来分析生铁中铁的含量.请你画出加入硫酸铜溶液质量与固体质量变化关系的曲线.
查看答案和解析>>
科目:初中化学 来源:2011年江苏省扬州地区中考化学三模试卷(解析版) 题型:解答题

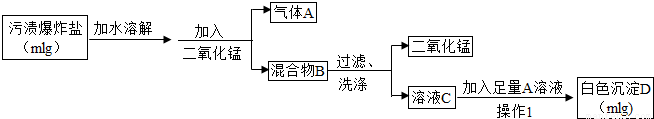
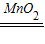 2H2O+O2↑
2H2O+O2↑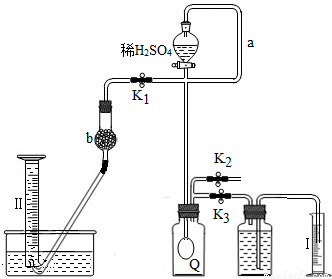
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com