
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量(g) | 0.3 | m | 0.9 | 1.0 | n |
分析 (1)根据取样品都是40g时,硫酸质量是30g时,生成氢气0.3g,硫酸是90g时,生成氢气是0.9g,所以硫酸是60g时,生成氢气是0.6g,硫酸是120g时,生成氢气1.0g,所以硫酸是150g时,生成的氢气也是1.0g进行分析;
(2)根据前3份反应中硫酸和氢气成正比,第4份加入120g硫酸生成氢气1.0g,与前3份中的数值不成正比,说明前三份中的硫酸完全反应进行分析;
(3)
解答 解:(1)取样品都是40g时,硫酸质量是30g时,生成氢气0.3g,硫酸是90g时,生成氢气是0.9g,所以硫酸是60g时,生成氢气是0.6g,硫酸是120g时,生成氢气1.0g,所以硫酸是150g时,生成的氢气也是1.0g,所以表中m的数值为0.6,n的数值应该为1.0;
(2)前3份反应中硫酸和氢气成正比,第4份加入120g硫酸生成氢气1.0g,与前3份中的数值不成正比,说明前三份中的硫酸完全反应;
(3)设40g样品中含锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 1.0g
$\frac{65}{x}$=$\frac{2}{0.1g}$
x=32.5g
所以黄铜样品中锌的质量分数为:$\frac{32.5g}{40g}$×100%=81.25%.
答:黄铜样品中锌的质量分数为81.25%.
故答案为:(1)0.6,1.0;
(2)1,2,3;
(3)81.25%.
点评 解答本题关键是要通过图表中数据分析出最多生成氢气1.0g,再利用方程式计算出锌的质量,再进一步进行计算.


科目:初中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 稀有气体可作保护气 | 原子核外电子达到相对稳定结构 |
| B | 物质热胀冷缩 | 分子大小随温度改变而改变 |
| C | 氧气和臭氧(O3)性质不完全相同 | 构成物质的分子不同 |
| D | 氧化汞受热分解为汞和氧气 | 在化学变化中分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.3g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 较多量液体加热--烧杯 | B. | 盛放固体药品--细口瓶 | ||
| C. | 少量试剂的反应--试管 | D. | 吸取和滴加少量液体--胶头滴管 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
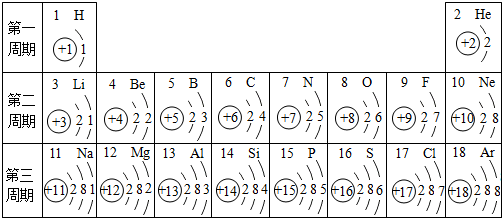
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
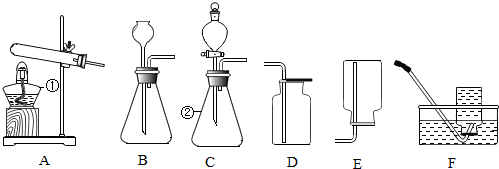
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
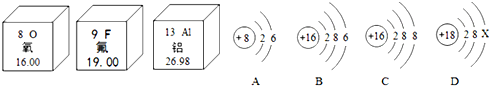
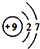 ,氟原子在化学反应中易得到(填“得到”或
,氟原子在化学反应中易得到(填“得到”或查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com