
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
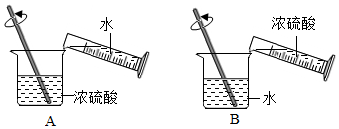
 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )| A. | 正极和负极产生的气体质量比为1:2 | |
| B. | 正极产生的气体能使带火星的木条复燃 | |
| C. | 每个水分子由两个氢原子和一个氧原子构成 | |
| D. | 水是由一个氧原子和氢原子组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
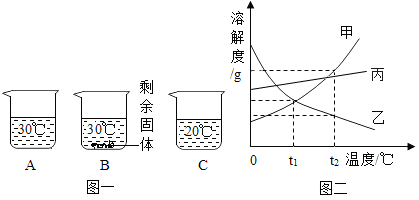
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 1987年8月,考古人员在南海海域意外地发现了一艘已经沉睡了800年,却至今仍未腐烂的古代沉船,2007年12月21日,“南海一号”古沉船被整体打捞.如图为整体打涝的情形.沉船打涝常用“浮筒打涝法”.首先把浮筒灌满水,沉入水底,拴在沉船两侧,然后再将筒内的水用高压气体压出,沉船便可以浮起来,“南海一号”顶出水面后,将放置到广东海上丝绸之路博物馆特别设置的“水晶宫”内.
1987年8月,考古人员在南海海域意外地发现了一艘已经沉睡了800年,却至今仍未腐烂的古代沉船,2007年12月21日,“南海一号”古沉船被整体打捞.如图为整体打涝的情形.沉船打涝常用“浮筒打涝法”.首先把浮筒灌满水,沉入水底,拴在沉船两侧,然后再将筒内的水用高压气体压出,沉船便可以浮起来,“南海一号”顶出水面后,将放置到广东海上丝绸之路博物馆特别设置的“水晶宫”内.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
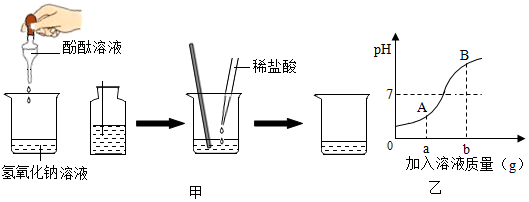
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中滴入Na2CO3溶液 | 产生气泡 | 猜想二成立 |
| 取少量反应后的溶液于试管中加入锌粒 | 没有气泡产生 | 猜想一成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com