
| A. | 食醋是一种酸 | |
| B. | 食醋中含有氢离子 | |
| C. | 食醋是一种混合物 | |
| D. | 可以从食醋中闻到酸味证明醋酸有挥发性 |
分析 A、根据酸是指在电离时产生的阳离子全部是氢离子的化合物,进行分析判断.
B、根据酸是指在电离时产生的阳离子全部是氢离子的化合物,进行分析判断.
C、根据食醋中含有醋酸、水,属于混合物,进行分析判断.
D、根据从酸中闻到酸味,进行分析判断.
解答 解:A、食醋中含有醋酸和水,属于混合物,而酸是指在电离时产生的阳离子全部是氢离子的化合物,故选项说法错误.
B、食醋中含有醋酸,醋酸中含有氢离子,故选项说法正确.
C、食醋中含有醋酸、水,属于混合物,故选项说法正确.
D、醋酸具有挥发性,可以从食醋中闻到酸味,证明醋酸有挥发性,故选项说法正确.
故选:A.
点评 本题难度不大,掌握酸的特征、食醋的组成成分的等是正确解答本题的关键.


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:初中化学 来源: 题型:解答题
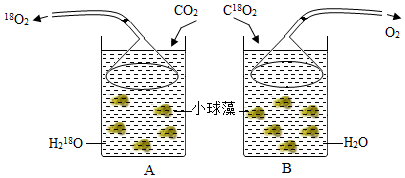 同位素示踪法是利用放射元素作为示踪剂,对研究对象进行标记的分析方法,用以研究化学、生物或其他过程.同位素示踪法的应用,使人们可以从分子水平动态地观察生物体内或细胞内生理过程,认识生命活动的物质基础.例如,用14C(一种质子数和中子数之和为14的碳原子)、18O(一种质子数和中子数之和为18的氧原子)等同位素研究光合作用,可以详细地阐明叶绿体如何利用二氧化碳和水,这些简单分子形成糖类等大分子的中间产物是什么,以及影响每步生物合成的反应条件等.
同位素示踪法是利用放射元素作为示踪剂,对研究对象进行标记的分析方法,用以研究化学、生物或其他过程.同位素示踪法的应用,使人们可以从分子水平动态地观察生物体内或细胞内生理过程,认识生命活动的物质基础.例如,用14C(一种质子数和中子数之和为14的碳原子)、18O(一种质子数和中子数之和为18的氧原子)等同位素研究光合作用,可以详细地阐明叶绿体如何利用二氧化碳和水,这些简单分子形成糖类等大分子的中间产物是什么,以及影响每步生物合成的反应条件等.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
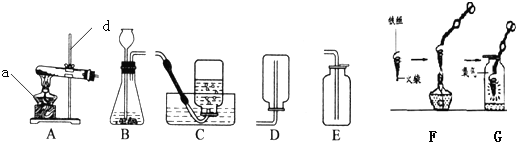
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
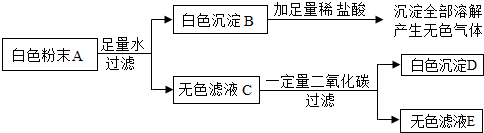
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
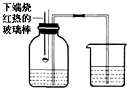 某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com