
���� ��1���Ȼ��Ƶ��ܽ�����¶ȵ�Ӱ�첻�����һ����������ܼ��ķ����õ��Ȼ��ƾ��壻
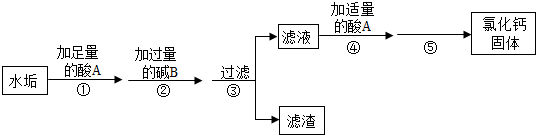
��2������Ӳˮ�����ķ������ǣ�
��3��������ˮ���������Ȼ��ƣ���10%��NaCl��Һ������100g 0.9%���Ȼ�����Һ����Ũ��ϡ�����ʲ��䣻
��4��������ҺpHʱ��������ˮ��pH��ֽ��ʪ����ý����ȷ��
��5������̼�������Ȼ�����Ӧ�Ļ�ѧ����ʽ�����ɳ������������г�����ʽ���Ϳɼ������Ӧ�����Ȼ��Ƶ�������Ȼ����ݡ�������������=$\frac{��������}{��Һ����}$��100%�����㼴�ɣ�
��� �⣺��1���Ȼ��Ƶ��ܽ�����¶ȵ�Ӱ�첻�����һ����������ܼ��ķ����õ��Ȼ��ƾ��壻
��2��Ӳˮ�����ķ����У�������к������õ��Ǽ�����У�
��3��������ˮ���������Ȼ��ƣ���10%��NaCl��Һ������100g0.9%���Ȼ�����Һ����Ũ��ϡ�����ʲ��䣬������ˮ������Ϊx����100g-x����10%=100g��0.9%��x=91g��
��4��С��ͬѧ�ڲ�����ҺpHʱ��������ˮ��pH��ֽ��ʪʱ���ٵμӴ���Һ��ʹ��Һ��������������С����������Һ��˵�����Լ���pHֵ����Լ���Һ���෴�������жϣ�
��5����Ӧ�����ɵij���������=100g+153.7g-234g=19.7g��
�跴Ӧ�����Ȼ��Ƶ�����Ϊx��
Na2CO3+BaCl2=2NaCl+BaCO3��
117 197
x 19.7g
$\frac{117}{197}=\frac{x}{19.7g}$
��x=11.7g��
����������Һ�е����ʵ���������Ϊ��$\frac{11.7g}{234g}$��100%=5%��
�𣺹���������Һ�е����ʵ���������Ϊ5%��
�ʴ�Ϊ��
��1����ɹ
��2�����
��3��91
��4����ȷ��
��5��5%
���� Ҫ�����������Ŀ�����ȣ�Ҫ�������ǿα��ϵ�һЩ����֪ʶ��


 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼����������Ƽ� | B�� | �ɱ������˹����� | ||
| C�� | �����������ڸ����������� | D�� | Ũ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����֭��ʹ��ɫʯ����Һ��� | B�� | У�����ʺ��ڴ����ֲ������� | ||
| C�� | ��������������Һ����У���� | D�� | �����ḯʴ����ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 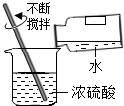 ϡ��ϡ���� | B�� | 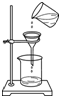 ���� | C�� | 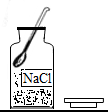 ȡ����ҩƷ | D�� | 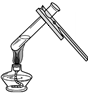 ����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
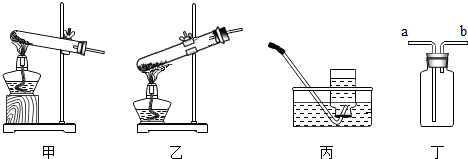
| ʵ�鲽�� | ����ʱ�䣨min�� | ʵ������ |
| �ٽ��������̵��������Թ��м��ȣ��������ǵ�ľ�������Թܿ� | 10 | ľ���ޱ仯 |
| �ڽ�����ص��������Թ��м��ȣ��������ǵ�ľ�������Թܿ� | 5 | ľ����ȼ |
| �۽�����ء��������̻�Ϸ����Թ��м��ȣ������ǵ�ľ�������Թܿ� | 1 | ľ����ȼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ļ�ռ�����ʯ�� | |
| B�� | �ϳɲ��ϣ��Ͻ𡢺ϳ����ϳ���ά | |
| C�� | ������Ӫ���أ������ʡ�ˮ��ά���� | |
| D�� | �л�����顢�Ҵ���̼�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com