
【题目】下列各组物质,只用无色酚酞试液及相互反应就能区别开来的是( )
A. NaOH、HCl、![]() B. NaOH、HCl、NaCl
B. NaOH、HCl、NaCl
C. ![]() 、HCl、NaClD. NaOH、
、HCl、NaClD. NaOH、![]() 、
、![]()
【答案】BC
【解析】
A、氢氧化钠溶液呈碱性,能使酚酞试液变红,盐酸和硫酸都呈酸性,都不能使酚酞试液变色,因此向三种溶液中滴加酚酞变红色的是氢氧化钠,无变化的是盐酸和硫酸,不能区别盐酸和硫酸,选项错误;
B、氢氧化钠溶液呈碱性,能使酚酞试液变红,盐酸呈酸性,氯化钠溶液呈中性,都不能使酚酞试液变色,分别向三种溶液中滴加酚酞试液,变红色的是氢氧化钠,无变化的是盐酸和氯化钠,取不变红的溶液中的一种滴入变红的溶液中,若红色消失,则滴加的为盐酸,若不消失,则滴加的为氯化钠,可以区分,选项正确;
C、碳酸钠溶液呈碱性,能使酚酞试液变红,取剩余的两种溶液中的一种滴入碳酸钠中,若产生气泡则该溶液为盐酸,反之为氯化钠,选项正确;
D、氢氧化钠、氢氧化钙、氢氧化钡溶液都呈碱性,都能使酚酞试液变红,故不能区别,故选BC。


科目:初中化学 来源: 题型:
【题目】下列实验数据合理的是( )
①用托盘天平称取![]() 氧化铜粉末 ②用
氧化铜粉末 ②用![]() 量筒量取
量筒量取![]() 的稀硫酸
的稀硫酸
③用普通温度计测得某液体的温度为![]() ④用
④用![]() 量筒量取某溶液
量筒量取某溶液![]()
A.①②B.②③④C.③④D.①④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】认识溶液的变化。根据如图甲、乙、丙三种固体的溶解度曲线回答:
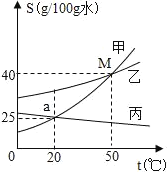
①M点表示的含义是_____。
②50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为_____。
③20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数_____(填“变大”、“变小”或“不变”)。
④分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案,不能达到相应实验目的的是( )
|
|
|
|
A.测定空气中氧气的含量 | B.验证质量守恒定律 | C.探究燃烧条件之一:温度达到着火点 | D.探究物质溶解性的影响因素 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语(即符号)表示:
(1)氢离子_____
(2)氢氧根离子_____
(3)碘酒中的溶剂_____
(4)H2SO4中硫元素的化合价_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某金属冶炼厂的管道烟泥中含有Cu、Zn及炭黑,现欲回收铜和锌,主要流程如图所示:
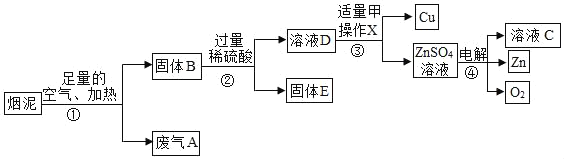
(1)步骤①产生的废气A中,一定含有的气体是_____。
(2)溶液D中一定含有的溶质是_____。
(3)步骤③中发生反应的化学方程式是_____(任写一个)。操作X的名称是_____;其所需玻璃仪器除漏斗、玻璃棒外,还有_____。
(4)步骤④中参加反应的物质为ZnSO4和_____(填化学式)。
(5)有人认为若步骤①中空气不足量,会导致锌的回收率降低,你认为是否正确?_____(填“正确”或“不正确”),理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答下列问题:
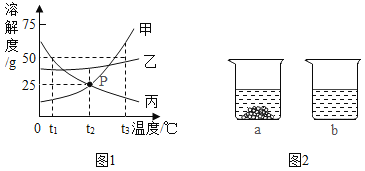
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是_________。
(2)P点表示,t2℃时,甲、丙两种物质的饱和溶液中,溶质与溶剂的质量比相等,均为_____。
(3)t2℃时,取甲、乙两种固体各15g分别加入40g水中充分溶解,实验现象如图2所示,
则烧杯a中溶解的物质是________(填“甲”或‘‘乙”),所得溶液的质量为______g。
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用______(填(“降温”或“蒸发”)结晶的方法提纯甲物质。
(5)下列说法正确的是____(填字母序号)。
A 将甲物质的溶液由t3℃降温到t2℃,一定有晶体析出
B 将甲物质的饱和溶液由t2℃升温至t3℃时,其溶质质最分数增大
C 将t3℃时三种物质的饱和溶液恒温蒸发等质量的水,析出溶质的质量:甲>乙>丙
D 将t3℃三种物质的饱和溶液降温至t2℃,所得溶液的溶质质量分数:乙>甲=丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为M、N两种固体物质的溶解度曲线,据图回答:
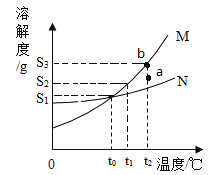
(1)b点表示的意义是_______。
(2)t2℃时,将M溶液的状态由a点转化到b点,可采用的方法是_______和_______。
(3)将t1℃时,M和N的饱和溶液各100g降温至t0℃,过滤,得到滤液m和滤液n。关于m和n的说法正确的是______(填序号)。
A 都是饱和溶液 B 溶液质量:m<n C 溶剂质量:m<n D 溶质质量:m=n E 溶质的质量分数:m=n
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究.
(查阅资料)
①NaN3受撞击会生成Na、N2.
②NaN3遇盐酸、H2SO4溶液没有气体生成.
③碱石灰是CaO和 NaOH的混合物.
④NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和NH3.
(问题探究)
(1)汽车经撞击后,30毫秒内引发NaN3迅速分解,写出该反应的化学方程式_____.
(2)工业级NaN3中常含有少量的Na2CO3,其原因是_____(用化学方程式表示).
(3)为测定某工业级NaN3样品中含有Na2CO3的质量分数,小组同学设计了如图实验装置.
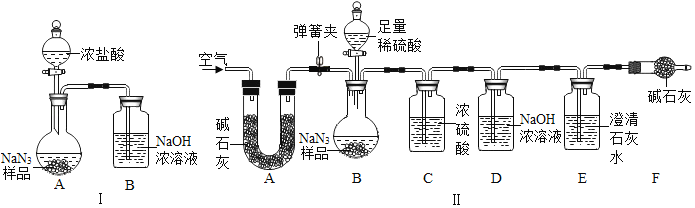
①小明同学认为通过测定装置Ⅰ中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组同学通过讨论装置Ⅰ认为很多因素会导致测定数据不准确,误差太大.小明同学在大家讨论的基础上,又设计了装置Ⅱ.请装置Ⅱ中A的作用是_____;若无装置C,对测定结果造成的影响是_____(填“偏大”、“偏小”或“无影响”);装置E的作用是_____.
②根据装置Ⅱ,小组同学设计的实验步骤有:
a.称量装置
b.称量样品,检查装置气密性.
c.打开弹簧夹,鼓入空气.
d.关闭弹簧夹,打开分液漏斗的活塞和玻璃塞,注入足量的稀硫酸,关闭活塞和玻璃塞.
为保证测定结果精确,正确的操作顺序为_____(填字母序号,可重复).
③计算碳酸钠的质量分数时,至少需要测定_____个数据.(填数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com