A
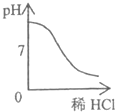
分析:A、根据NaOH溶液与盐酸的反应时溶液的酸碱度的变化分析;
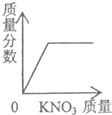
B、根据向接近饱和的KNO3溶液中加入KNO3时溶液的溶质的质量分数的变化分析;
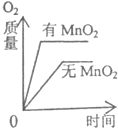
C、根据催化剂的定义分析;
D、根据CuSO4与NaOH的反应分析.
解答:A、NaOH溶液的pH大于7,当加入盐酸时,与氢氧化钠反应,溶液的pH逐渐减小,当盐酸过量时,pH小于7,故A正确;
B、接近饱和的KNO3溶液中溶质的质量分数不能等于0,故B错误;
C、由催化剂的定义可知,催化剂改变的是反应的速率,不能改变生成氧气的质量,生成的氧气的应质量相等,故C错误;
D、向一定量的CuSO4溶液里滴加NaOH溶液时生成的氢氧化铜沉淀,当CuSO4全部参加反应时生成的沉淀的质量达到了最大,不可能无限地增加,故D错误.
故选A.
点评:此题是过程与图象结合题,是对学生识图能力的考查,解题的关键是能正确的分析各个反应的过程,并结合图象分析问题,对培养学生分析问题的能力有一定帮助.




 小学课时特训系列答案
小学课时特训系列答案