
【题目】下列说法正确的是( )
A. 铁、锌、钙、硒、碘都是人体必需的微量元素
B. 厨房内煤气泄漏后应该立即开启排气扇通风,以免发生中毒事故
C. 若“![]() ”表示氧原子,则“
”表示氧原子,则“![]() ”和“
”和“![]() ”都表示的是化合物,且都是氧化物
”都表示的是化合物,且都是氧化物
D. 用氯化钠固体配制 50g 20%的氯化钠溶液时,量水时仰视或称量的氯化钠药品不纯,均使所配溶液中溶质的质量分数减小
科目:初中化学 来源: 题型:
【题目】现有一定质量的硝酸钠和氯化钠的混合物,其中含钠元素9.2g。将此混合物加足量水配成溶液,再加入一定量硝酸银溶液,恰好完全反应,生成氯化银白色沉淀28.7g。计算:
(1)原混合物中氯化钠的质量_______;
(2)原混合物中硝酸钠的质量分数(结果保留至0.1%)___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将含有可溶性杂质的某氯化钠样品3g溶于足量水中得到不饱和溶液,再向所得溶液中小心滴入200g一定溶质的质量分数的AgNO3溶液(杂质不与AgNO3溶液反应)。实验过程中,生成沉淀的质量与滴入AgNO3溶液的质量关系如右图所示。试计算:
(提示:NaCl + AgNO3 = AgCl↓+ NaNO3 )

(1)恰好完全反应时生成沉淀质量为 g;
(2)硝酸银溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
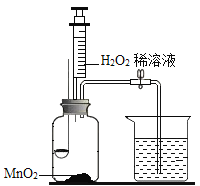
【题目】某同学用如图所示装置.分别进行“燃烧条件”和“氧气性质”的探究实验(已知:白磷的着火点为40℃)。请回答下列问题:
内容步骤 | (实验1)燃烧条件 | (实验2)氧气性质 |
1 | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞; | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞; |
2 | 推入H2O2溶液 | 推入H2O2溶液 |
(1)H2O2与MnO2接触时,发生反应的化学方程式为___________________,MnO2起_________作用。
(2)实验1中,推入H2O2溶液,燃烧匙和水中的白磷均不燃烧,原因分别是___、____;打开止水夹,推入H2O2溶液,观察到烧杯中的现象是_______。
(3)实验2中打开止水夹,推入H2O2溶液,观察到木炭燃烧得更剧烈,由此得出氧气的性质是_______,木炭熄灭冷却一段时间后,烧杯中的部分溶液流入集气瓶,该实验开始时到实验结束后,集气瓶内压强的变化过程是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合图示实验装置,回答下列问题。
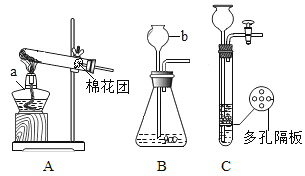
(1)用A装置制取氧气,发生的化学反应方程式为_____,若用B装置制取气体,为了控制反应的速率,应将长颈漏斗改为_____。
(2)用装置C制取气体时,关闭导气管上的活塞,过一会儿反应就会停止,其原因是_____。用C装置在实验室制取CO2时,发生的化学反应方程式为_____;若用铁丝网代替多孔隔板,则产生新增杂质气体的化学反应方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组为验证“氨气还原氧化铜”的实验,认真查阅资料并做出以下准备。
资料准备:
I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气在加热的条件下还原氧化铜,有三种生成物:一是金属单质,二是空气中含量最多的气体,三是相对分子质量最小的氧化物。
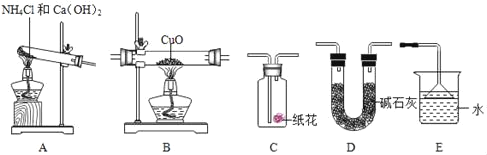
实验准备:
请回答:
(1)为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序_____(填序号)。
(2)装置A中发生反应的化学方程式_____。
(3)装置B观察到的现象_____,其反应的化学方程式为_____;装置E的作用_____。
(4)若将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变_____色。
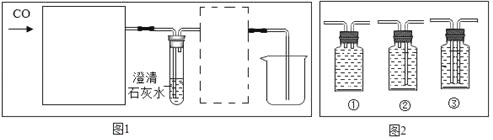
(5)若实验室用一氧化碳还原氧化铜,应选上述装置_____(填序号)与下列图1中的_____装置连接,则该装置玻璃管内发生反应的化学方程式是_____,实验时要先通CO再加热的目的是防止一氧化碳和空气混合加热时发生爆炸。图1虚线框内的装置是用于吸收CO2,并收集CO,应选择图2(广口瓶内均为氢氧化钠溶液)中的装置_____(填序号)最合适。
查看答案和解析>>
科目:初中化学 来源: 题型:
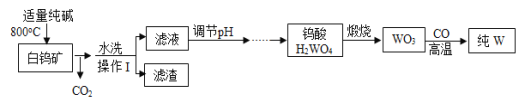
【题目】白钨矿的主要成分是CaWO4,工业上用白钨矿生产钨的流程如图所示:
(查阅资料)
CaWO4与纯碱发生反应的化学方程式是CaWO4+Na2CO3═Na2WO4+CaO+CO2↑。
(1)反应前需要将白钨矿进行粉碎,其目的是_____;
(2)水洗后进行的分离操作中,所用的玻璃仪器有烧杯、_____和玻璃棒,其中玻璃棒的作用是_____;
(3)上述滤液的成分中含有氢氧化钙,写出生成该物质的反应的化学方程式:_____;
(4)三氧化钨与氢气反应时,表现出还原性的物质是_____写出金属钨的一种用途:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )
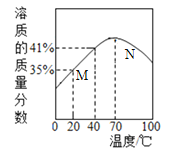
A. N 点对应的 ZnSO4 溶液升温或降温均都可能析出晶体
B. M 点对应的 ZnSO4 溶液是不饱和溶液
C. ZnSO4 饱和溶液的溶质质量分数随温度升高而增大
D. 40℃时,ZnSO4 的溶解度为41g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如图所示。

(1)甲和乙两种物质的溶解度随温度的升高而____(填“增大”或“减小”);
(2)下列对P点的含义叙述正确的是____(填序号);
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
(3)25 g乙物质完全溶于100 g水中所需的最低温度是____℃;
(4)t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,需蒸发掉较多水的是____(填“甲”或“乙”)物质饱和溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com