
| A. | 叶酸的相对分子质量为441 g | |
| B. | 叶酸中氮元素的质量分数大于氧元素的质量分数 | |
| C. | 叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6 | |
| D. | 叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成 |
分析 A.根据相对分子质量的单位来分析;
B.根据化合物中元素的质量比来分析;
C.根据化合物中元素质量比的计算方法来分析;
D.根据物质的构成来分析.
解答 解:A.相对分子质量的单位不是“g”而是“1”,通常省略不写,故错误;
B.叶酸(Cl9Hl9N7O6)中氮、氧元素质量比为(14×7):(16×6)=98:96,可见其中氮元素的质量分数大于氧元素的质量分数,故正确;
C.叶酸中碳、氢、氮、氧四种元素质量比为(12×19):(1×19):(14×7):(16×6)≠19:19:7:6,故错误;
D.叶酸是由分子构成的而不是由原子直接构成的,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:初中化学 来源: 题型:选择题
| A. | 城市道路定时洒水降尘 | B. | 公共场所禁止吸烟 | ||
| C. | 建筑工地加强扬尘控制 | D. | 垃圾露天焚烧处理 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1滴水中大约有1.67×1021个水分子 | |
| B. | 空气被压缩后体积缩小 | |
| C. | 2L氢气和氧气的混合气体点然后体积小于2L | |
| D. | 满架蔷薇一院香 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | B. | H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑ | ||
| C. | NaOH+HCl═NaCl+H2O | D. | 2Al+6HCl═2AlCl3+3H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2个铝离子:2Al3+ | B. | 钠原子的结构示意图: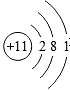 | ||
| C. | 氧分子:O | D. | 氧化镁中镁元素显+2价:$\stackrel{+2}{Mg}$O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热试管内的碱式碳酸铜,绿色粉末逐渐变黑,试管口有小水滴 | |
| B. | 细铁丝在氧气中燃烧,火星四射,生成红棕色固体 | |
| C. | 镁条在空气中燃烧,产生黑烟,生成黑色粉末 | |
| D. | 向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某初级中学学生为探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如右图所示)可能是什么物质,大胆猜想并设计实验进行验证.
某初级中学学生为探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如右图所示)可能是什么物质,大胆猜想并设计实验进行验证.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 玻璃管质量m0/g | 玻璃管与钙的质量m1/g | 玻璃管与产物的质量m2/g |
| 14.80 | 15.08 | 15.25 |
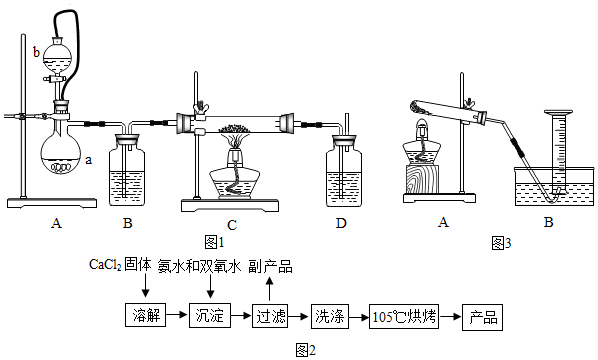
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com