
| 56 |
| x |
| 2 |
| 0.2g |
| 5.6g |
| 5.8g |


科目:初中化学 来源: 题型:
| +2 |
| Fe |
| +2 |
| Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:
 ”表示氢原子,用“○○”表示氧原子,请回答:
”表示氢原子,用“○○”表示氧原子,请回答:
 表示的分子的化学式是
表示的分子的化学式是
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:022
(2005
年江西)用化学用语填空:(1)
磷元素________;(2)2
个银原子________;(3)3
个氮分子________;(4)
碱中的阴离子________;(5)
氧化亚铁中铁元素显+2价________.查看答案和解析>>
科目:初中化学 来源: 题型:058
(2005
年江西)“绿色化学”强调实验设计应采取有效措施,节约能源、防止对环境的破坏和污染.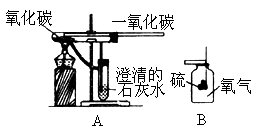
(1)
图A是小欣同学设计的一氧化碳还原氧化铁的实验.该实验符合“绿色化学”要求,体现在:为了防止污染,通过燃烧除去未反应完的__________,充分利用其燃烧产生热量,节约能源;(2)
写出图B中发生反应的化学方程式_________,该实验不符合“绿色化学”要求,这是因为反应产物会逸散而污染空气,请你就此实验设计一个消除或减少污染的方法____________________________.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com