
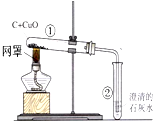
 实验室用木炭还原氧化铜的实验,请回答
实验室用木炭还原氧化铜的实验,请回答
| ||
| ||


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 公共汽车 | 出租车 | |
| 百公里耗油/kg | 18 | 9 |
| 平均载客量/人 | 30 | 3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、6H | B、6B | C、HB | D、2B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com