
| A. | 石蕊试液 | B. | 稀盐酸 | C. | 氢氧化钠稀溶液 | D. | 碳酸钠溶液 |
分析 根据三种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
解答 解:A、紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,硫酸、氢氧化钙和氯化钠三种无色稀溶液分别显酸性、碱性、中性,使石蕊溶液分别显示红色、蓝色、紫色,能出现三种明显不同的现象,故可以鉴别.
B、稀盐酸能与氢氧化钙反应生成氯化钙和水,但无明显变化;与硫酸、氯化钠均不反应,不能出现三种明显不同的现象,故不能鉴别.
C、氢氧化钠稀溶液与硫酸反应生成硫酸钠和水,但无明显变化;与氢氧化钙和氯化钠均不反应,不能出现三种明显不同的现象,故不能鉴别.
D、碳酸钠溶液与硫酸反应产生二氧化碳气体,与氢氧化钙反应产生碳酸钙白色沉淀,与氯化钠不反应;分别滴加Na2CO3溶液,产生气泡的是硫酸,产生白色沉淀的是氢氧化钙溶液,无明显变化的是氯化钠溶液;能出现三种明显不同的现象,故可以鉴别.
故选:AD.
点评 本题有一定难度,在解决鉴别物质题时,判断的依据是:所选试剂需要与待鉴别的物质反应并出现明显不同的现象.


科目:初中化学 来源: 题型:填空题
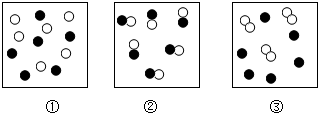 如图①、②、③分别为某些分子或原子的示意图,其中黑、白两种圆圈分别代表汞原子(Hg)和氧原子(O).请用各图对应的序号回答下列问题.
如图①、②、③分别为某些分子或原子的示意图,其中黑、白两种圆圈分别代表汞原子(Hg)和氧原子(O).请用各图对应的序号回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 框图中B用于改良酸性土壤,J是最常见的金属,G是红棕色物质,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝,在溶液D中滴入AgNO3溶液产生难溶于硝酸的白色沉淀.
框图中B用于改良酸性土壤,J是最常见的金属,G是红棕色物质,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝,在溶液D中滴入AgNO3溶液产生难溶于硝酸的白色沉淀.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质的类别 | 氧化物 | 酸 | 碱 | 盐 |
| 物质的化学式 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
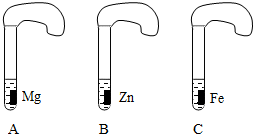 一般情况下,金属越活泼,与酸反应的速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下的实验.
一般情况下,金属越活泼,与酸反应的速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下的实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com