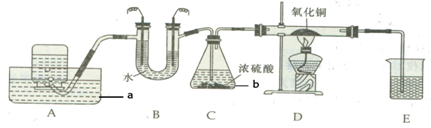
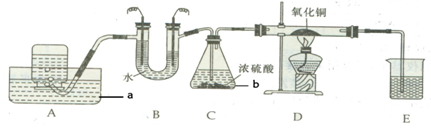
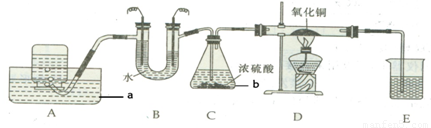
解:(1)图中有标号的仪器名称为a 水槽,b 锥形瓶.
(2)正极产生氧气,负极产生氢气,氧气与氢气的体积比为 1:2.
(3)要证明氢气还原氧化铜的产物水,可用无水硫酸铜,若有水产生,则无水硫酸铜变蓝,因此要将上述装置改动.把E改为装有无水硫酸铜的U形管或干燥管.
(4)上述改动后实验过程中所发生的化学方程式为 H
2+CuO

Cu+H
2O CuSO
4+5 H
2O=CuSO
4.5H
2O;2H
2O

2 H
2↑+O
2↑
(5)根据水的物质的量可求出氧气的物质的量,根据氧气的物质的量,可求出氯酸钾的物质的量,从而求出氯酸钾的质量.
故答案为:(1)水槽 锥形瓶
(2)1:2
(3)要改动 把E改为装有无水硫酸铜的U形管或干燥管
(4)H
2+CuO

Cu+H
2O CuSO
4+5 H
2O=CuSO
4.5 H
2O
2H
2O

2 H
2↑+O
2↑
(5)解:设生成氧气的物质的量为x
2H
2O

2 H
2↑+O
2↑
2 1
3mol x

=
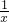
X=1.5mol
设需要氯酸钾物质的量为Y
2KClO
3
2KCl+3O
2↑2 3
Y 1.5mol
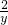
=
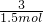
Y=1 mol
1mol×122.5g/mol=122.5克.
答.电解3mol水可以产生1.5摩尔的氧气这些氧气可分解122.5克的氯酸钾制得
分析:(1)根据仪器用途写出名称
(2)根据电解水实验的现象解答
(3)检验水用无水硫酸铜
(4)根据反应物生成物写出化学方程式
(5)根据化学方程式中已知物可求出特求物质的物质的量,进而求出质量.
点评:明确电解水用到的仪器、现象、水的检验方法及根据化学方程式计算的步骤是解答本题关健.

 Cu+H2O CuSO4+5 H2O=CuSO4.5H2O;2H2O
Cu+H2O CuSO4+5 H2O=CuSO4.5H2O;2H2O 2 H2↑+O2↑
2 H2↑+O2↑ Cu+H2O CuSO4+5 H2O=CuSO4.5 H2O
Cu+H2O CuSO4+5 H2O=CuSO4.5 H2O 2 H2↑+O2↑
2 H2↑+O2↑ 2 H2↑+O2↑
2 H2↑+O2↑  =
=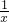
 2KCl+3O2↑
2KCl+3O2↑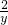 =
=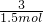


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
 2H2↑+O2↑
2H2↑+O2↑