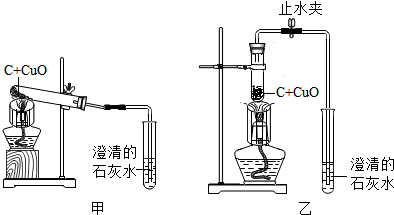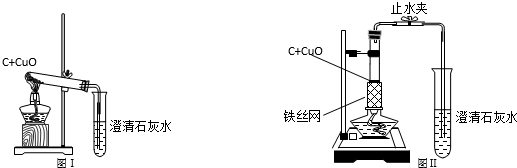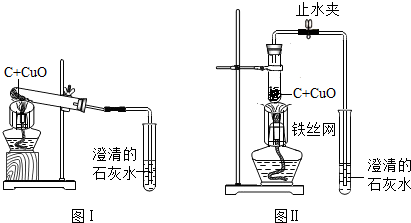
木炭作为还原剂用于金属冶炼已有几千年历史.教材用如图Ⅰ实验介绍这一知识.
(1)木炭与氧化铜反应的化学方程式是
;
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用.这样处理的目的是
增大反应物的接触面积,使反应更充分
增大反应物的接触面积,使反应更充分
;
(3)酒精灯火焰加有铁丝网罩,其作用是
使火焰更集中并提高温度
使火焰更集中并提高温度
;
(4)为了提高实验成功率,某研究小组设计如图Ⅱ方案进行实验.
[装置改进]
稳定的高温是本实验成功的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为直立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯高度.你认为该用酒精灯火焰的
外焰
外焰
(部位)加热;理由是
外焰温度最高
外焰温度最高
.
[实验研究]
分别称取2g木炭与不同质量的CuO混合,按每种比例重复实验3次.实验现象及查阅资料获得的实验结果记录如表:
不同比例的木炭与CuO实验对比表
| 比例 |
1:6 |
1:7 |
1:8 |
1:9 |
1:10-1:11 |
1:12 |
1:13 |
| 加热时间 |
1′51″ |
1′43″ |
1′57″ |
1′51″ |
1′51″ |
1′53″ |
4′ |
| 实验现象 |
红热,产生大量气泡,石灰水变浑浊 |
偶尔红热,气泡较少 |
| 实验结果 |
表层铜珠较大,出现未完全反应的黑色木炭烨末,且木炭含量越高黑色粉末越多 |
反应较完全,生成亮红色网状铜块 |
部分生成
Cu2O |
主要产物是
Cu2O |
由实验数据分析,影响实验的另一因素是
反应物的比例
反应物的比例
;从产物分析,该反应混合物的最佳比例范围是
1:10~1:11
1:10~1:11
.
[讨论交流]
由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,还能达到的目的是
排净试管内的空气
排净试管内的空气
;
②不能把石灰水变浑浊作为木炭跟CuO反应的充分依据.因为试管中还可能发生的反应是
(写化学方程式);
③小明认为用装置Ⅰ进行实验,还存在一定的问题,请你指出它的主要问题是
尾气没有处理,过程中可能产生的一氧化碳会污染环境
尾气没有处理,过程中可能产生的一氧化碳会污染环境
,改进的方法是
装石灰水的试管加上双孔橡皮塞,然后把尾气烧掉(或把排出一氧化碳的导管放在酒精喷灯下点燃或用气球收集起来)
装石灰水的试管加上双孔橡皮塞,然后把尾气烧掉(或把排出一氧化碳的导管放在酒精喷灯下点燃或用气球收集起来)
.
[拓展探究]关于影响该实验的因素,你认为还可进一步探究的问题有
反应物的形状(或反应温度)
反应物的形状(或反应温度)
.

 木炭作为还原剂用于金属冶炼已有几千年历史.教材用如图Ⅰ实验介绍这一知识.
木炭作为还原剂用于金属冶炼已有几千年历史.教材用如图Ⅰ实验介绍这一知识.