(2010?玉溪)把标准状况下1120mL二氧化碳气体(密度为1.977g/L)通入溶质质量分数为10%的氢氧化钠溶液中恰好完全反应,反应方程式:CO2+2NaOH=Na2CO3+H2O,
求(计算结果精确到0.1%):
(1)反应前溶质质量分数为10%的氢氧化钠溶液的质量;
(2)反应后所得溶液中溶质Na2CO3的质量分数.
【答案】
分析:根据化学方程式和二氧化碳的质量,列出比例式,即可计算出反应前溶质质量分数为10%的氢氧化钠溶液的质量和反应后所得溶液中溶质Na
2CO
3的质量分数.
解答:解:设反应前溶质质量分数为10%的氢氧化钠溶液的质量为x,反应后Na
2CO
3的质量为y,
CO
2 +2NaOH═Na
2CO
3+H
2O
44 80 106
1.12L×1.977g/L 10%x y
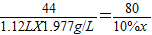
解之得:x=40g;
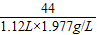
=
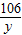
y=5.3g
反应后所得溶液的质量为:氢氧化钠溶液的质量+二氧化碳的质量=40g+1.12L×1.977g/L=40g+2.2g=42.2g
反应后所得溶液中溶质Na
2CO
3的质量分数为:

=12.6%.
答:(1)反应前溶质质量分数为10%的氢氧化钠溶液的质量是40g;
(2)反应后所得溶液中溶质Na
2CO
3的质量分数是12.6%.
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

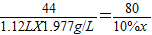
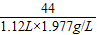 =
=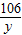
 =12.6%.
=12.6%.
