
��������������������Ӧ�ù㷺��
��1��������Ʒʹ�ý������ϵ��� ������ĸ��ţ��� ��2����Ȼ���еĽ�������Ի�������ʽ���ڣ���ȡ�������ʵķ����ж��֡���ҵ���ó�����ʯұ�����Ļ�ѧ����ʽΪ ������ұ�������л�ԭ��������ұ������õ�ⷨ��ͨ��ֽ����ڵ���������ȡ���Ļ�ѧ����ʽΪ ��
��2����Ȼ���еĽ�������Ի�������ʽ���ڣ���ȡ�������ʵķ����ж��֡���ҵ���ó�����ʯұ�����Ļ�ѧ����ʽΪ ������ұ�������л�ԭ��������ұ������õ�ⷨ��ͨ��ֽ����ڵ���������ȡ���Ļ�ѧ����ʽΪ ��
��3����ϧ�ͱ���������Դ�Ĵ�ʩ֮һ�Ƿ�ֹ������ʴ��ʹ�ù��IJ˵���ϴ����Ҫ��ʱ���ɷ��ã����Լ���________������ʴ��Ӱ�졣
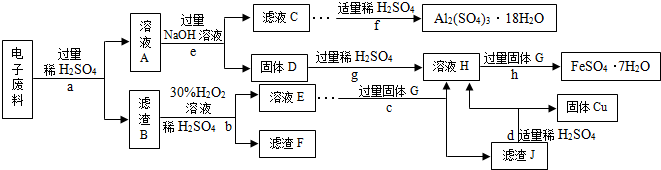
��4�����շϾɽ����DZ���������Դ����Ҫ��ʩ����ѧС���ͬѧ�ӵ��������л���˺�Cu 70%��Al 25%��Fe 4%������Au��Pt�ĵ��ӷ��ϣ��������»��մ�����ʡ�Է�������Ͳ��ֲ�Ʒ�����������������Ʒ����������Ԫ�أ����ش��й����⣺
�ٲ���c�ڼ������GǰӦ�ȳ�ȥ��Һ�еĹ������⣬��ȥ��������ļ����û�ѧ����ʽ��ʾΪ ��
����ҺA�к��е������� ��
��A~J���������У�������Ԫ�ص��� ������ĸ��ţ���
��1��AC ��2��3CO+Fe2O3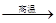 3CO2+2Fe ��2Al2O3
3CO2+2Fe ��2Al2O3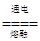 4Al + 3O2��
4Al + 3O2��
��3��H2O ��4����2H2O2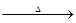 2H2O + O2�� ��Al2��SO4��3��H2SO4��FeSO4 ��ADGJH
2H2O + O2�� ��Al2��SO4��3��H2SO4��FeSO4 ��ADGJH
���������������1�������ˮ��ͷ����ͭ��������ɽ��������Ƴɣ���2����ҵ���ó������һ����̼�����·�Ӧ�������Ͷ�����̼����������������õ������ʺ���������3��������Ҫ��ͬʱ��������ˮ�Ӵ������ֱ��������Է�ֹˮ�Ĵ��ڣ���4���ٹ���������ȷֽ�����ˮ���������ڼ��������ϡ�������ҺA�е�����Ϊ���������ᣬ���������Ӧ���ɵ������������������Ӧ���ɵ�������������ADGJH�ж�������Ԫ�أ�������ͬһ�����У�������������ˮ����������
���㣺��ѧ����
����������֪ʶ�����п������ڱؿ����ͣ����ѣ�����Ӧע����ۣ��ر���һЩϸС�������֪ʶ�㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
| ||
| ���� |
| ||
| ���� |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com