
现有硫酸和硫酸铜的混合溶液124.9 g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀的质量与所加入的氢氧化钠溶液的质量关系如右图所示。求:
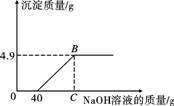
(1)恰好生成最大沉淀量时所加入的氢氧化钠溶液的总质量为____g;
(2)恰好生成最大沉淀量时所得溶液中溶质的质量分数。
80
 解:设与硫酸铜溶液反应的氢氧化钠溶液的质量为x,生成的硫酸钠的质量为y。
解:设与硫酸铜溶液反应的氢氧化钠溶液的质量为x,生成的硫酸钠的质量为y。
CuSO4+2NaOH=== Cu(OH)2↓+Na2SO4
Cu(OH)2↓+Na2SO4
80 98 142
x×10% 4.9 g y
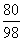 =
=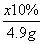 x=40 g
x=40 g
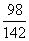 =
=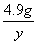 y=7.1 g
y=7.1 g
(1)依图可知,与H2SO4反应消耗氢氧化钠溶液为40 g,故生成最大沉淀量时,加入的氢氧化钠溶液总质量为:40 g+40 g=80 g。
(2)设NaOH与H2SO4反应生成的Na2SO4质量为z。
2NaOH+H2SO4===N a2SO4+H2O
a2SO4+H2O
80 142
40×10% z
 =
=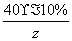 z=7.1 g
z=7.1 g
溶液中Na2SO4的质量分数= ×100%=7.1%
×100%=7.1%


 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:
如图所示,把同样大小的滤纸和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )
A.实验中使用铜片,是利用了铜的导热性
B.铜片受热的一面变黑,是因为产生了氧化铜
C.实验过程中滤渣碎片先燃烧,乒乓球碎片后燃烧
实验说明燃烧的条件之一是温度达到可燃物的着火点
 |
查看答案和解析>>
科目:初中化学 来源: 题型:
为了获取“铁的金属活动性比铜强”的证据,可以采用
A.比较铁的利用范围是否比铜广 B.观察铁是否能置换硫酸铜溶液中的铜
C.观察铁表面的锈迹是否比铜多 D.比较铁的相对原子质量是否比铜小
查看答案和解析>>
科目:初中化学 来源: 题型:
对比、分析、归纳是学习化学的重要方法。
(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuO Cu+H2O 3CO+Fe2O3
Cu+H2O 3CO+Fe2O3 2Fe+3CO2 C+O2
2Fe+3CO2 C+O2 CO2
CO2
得出的结论:物质(如H2、C O、C)作还原剂时,所含元素中,一定有元素的化合价在反应后__ __(填“
O、C)作还原剂时,所含元素中,一定有元素的化合价在反应后__ __(填“ 升高”“降低”或“不变”)。
升高”“降低”或“不变”)。
(2)依据上述结论,则在反应SO2+2H2S===3S+2 H2O中作为还原剂的物质是_ __;该还原剂中所含元素化合价的变化是由___变为___。
H2O中作为还原剂的物质是_ __;该还原剂中所含元素化合价的变化是由___变为___。
查看答案和解析>>
科目:初中化学 来源: 题型:
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。

(1)向固体乙上滴加盐酸时__ _(填“有”或“没有”)气泡产生。
(2)溶液甲中一定含有哪些溶质?__ __。(写化学式)
(3)请写出该实验过程中所发生反应的化学方程式
__ _。
查看答案和解析>>
科目:初中化学 来源: 题型:
A、B、C、D是实验室常见的四种物质,A、B、C在一定条件下的转化关系如图所示。在C溶液中通入CO2,溶液变浑 浊,生成白色沉淀A。D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀。请回答:
浊,生成白色沉淀A。D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀。请回答:
(1)写出B、C的化学式:B_ _;C_ _。
(2)C转化成A的化学方程式为_;D与A反应的化学方程式为_ _;基本反应类型是_ _。
查看答案和解析>>
科目:初中化学 来源: 题型:
A、B、C、D、E、F及甲、乙均为初中化学常见物质,请回答下列问题:

(1)甲为氧化物,能与溶液A反应得到黄色溶液,则甲的化学式为_ _。
(2)乙为厨房中常用的调味 品,可由A、B两种溶液发生中和反应得到,则A与B反应的化学方程式为_ _。
品,可由A、B两种溶液发生中和反应得到,则A与B反应的化学方程式为_ _。
(3)固体C常用于改良酸性土壤,且C与D反应可得到B,该反应属于基本类型中的_ _,其中D的化学式为_ _;指出D的一种用途_ _。
(4)已知上述物质间存在如图所示的关系(“→”表示转化关系;“—”表示反应关系),其中E与F的物质类别相同,则E的化学式为_ _,F与C反应的化学方程式为_ _。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列各组物质在溶液中能大量共存且形成无色溶液的是( )
A.NaCl、BaCl2、Na2CO3
B.KNO3、HCl、CaCl2
C.H2SO4、FeCl3、NaNO3
D.NaOH、HNO3、NH4NO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com