
(7分)菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究。取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如下表:
加入H2S04溶液的质量/g | 50 | 100 | 150 | 200 |
NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
说明:菱镁矿中的杂质不溶于水,不与酸发生反应。.
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为 。
(2)计算该菱镁矿中镁元素的质量分数。(写出计算过程)

(3)该实验研究中所用H2SO4溶液的溶质的质量分数是 。
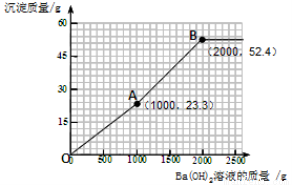
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的Ba(OH)2溶液。请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图。(在答题卡的坐标中作图,并标出曲线折点的坐标)
(1)4.4g
(2)菱镁矿中镁元素的质量分数为24%。
(3)9.8%
(4)作图见下图曲线
【解析】
试题分析:(1)碳酸镁可与稀硫酸反应生成二氧化碳气体,氢氧化钠可与二氧化碳气体反应。所以氢氧化钠溶液增重的质量即为反应生成的二氧化碳的质量。由于氢氧化钠溶液增重的质量最大值为4.4g 。所以生成CO2的质量为4.4g。
(2)根据题意可知:已知量为生成二氧化碳的质量;未知量为菱镁矿中镁元素的质量分数。解题思路:可根据二氧化碳与碳酸镁在反应体系中的质量关系,求出碳酸镁的质量。再进一步可计算出菱镁矿中镁元素的质量分数。具体过程如下:
解:设菱镁矿中MgCO3的质量为x。
MgCO3+H2SO4=MgSO4+H2O+CO2↑
84 44
x 4.4g
84∶44=x∶4.4g
x = 8.4g
菱镁矿中镁元素的质量分数=[(8.4g×24/84)÷10g]×100%?24%
答:该菱镁矿中镁元素的质量分数为24%。
(3)根据表格中的数据可知:第一、二两次中的硫酸完全反应,所以可根据第一、二两次中二氧化碳的质量计算出参加反应的硫酸的质量,进一步计算出硫酸的质量分数。具体过程如下:
解:设所用H2SO4溶液的溶质的质量分数为y
MgCO3+H2SO4=MgSO4+H2O+CO2↑
98 44
100gy 4.4g
98:44=100gy:4.4g
y = 9.8%
所用H2SO4溶液的溶质的质量分数为9.8%。
(4)加入的氢氧化钡可先与过量的稀硫酸反应。由于过量的稀硫酸中硫酸的质量为(200g—100g)×9.8%= 9.8g。根据反应的化学方程式可计算出:可恰好反应掉氢氧化钡溶液的质量为1000g,同时生成硫酸钡沉淀的质量为23.3 g。所以图像中的第一个折点的坐标为(1000,23.3 )。
再加入的氢氧化钡与硫酸镁反应。根据反应的化学方程式可计算出:硫酸镁的质量为12 g,可恰好反应掉氢氧化钡溶液的质量为1000g,同时生成硫酸钡沉淀的质量为23.3 g,生成氢氧化镁沉淀的质量为5.8 g。因此图像中的第二个折点所用的氢氧化钡溶液的质量为1000 g+1000 g=2000 g。同时沉淀的质量为23.3 g+23.3 g+5.8 g=52.4 g。所以图像中的第二个折点的坐标为(2000,52.4)。
再加入氢氧化钡时,不再产生沉淀。可根据规律进行描点和画图为: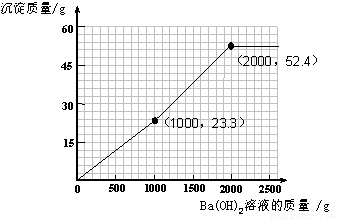
考点:根据化学方程式的计算


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:初中化学 来源:2014年初中毕业升学考试(广西玉林、防城港卷)化学(解析版) 题型:选择题
某粗盐固体样品中含有少量CaCl2、MgCl2、Na2SO4、MgSO4和泥沙,进行以下操作可得到纯净的NaCl晶体:①加过量的NaOH溶液;②加H2O溶解;③加过量的BaCl2溶液;④过滤;⑤蒸发;⑥加过量的Na2CO3溶液;⑦加适量的稀盐酸,则正确的操作顺序是( )
A.②①⑥③④⑦⑤ B.②①③⑥⑦④⑤
C.①⑥②③④⑤⑦ D.②③①⑥④⑦⑤
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试(广西崇左市卷)化学(解析版) 题型:选择题
下列实验现象描述不正确的是( )
A.纯羊毛制品点燃后有烧焦羽毛气味产生
B.黄铜片与铜片互相刻画,黄铜片可以在铜片上画出痕迹
C.硫在空气中燃烧产生明亮的蓝紫色火焰,生成有刺激性气味的气体
D.将少量熟石灰粉末与硝酸铵固体混合、研磨,能嗅到强烈的刺激性气味
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试(广东茂名卷)化学(解析版) 题型:选择题
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )

A.T2℃时甲和乙的饱和溶液,降到T1℃时,甲乙仍是饱和溶液且有晶体析出
B.甲和乙的溶解度相等
C.T1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液
D.T2℃时,100g甲的饱和溶液里含有溶质甲的质量为50g
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试(广东省佛山卷)化学(解析版) 题型:推断题
(7分)A—G是初中化学常见物质。其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀。下图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。

(1)请写出化学式:A ,F 。
(2)写出D→E的化学方程式:
。
(3)在A→E的反应过程中,A与G溶液恰好完全反应,反应后所得溶液的pH 7(填“>”、“=”或“<”)。
(4)C溶液与铁粉反应后,取剩余固体加入盐酸,没有气体放出。请分析:C与铁粉反应后的溶液组成中除了H2O外,一定存在的物质有 ,可能存在的物质有 。
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试(广东省佛山卷)化学(解析版) 题型:选择题
下列各组物质中都有三种溶液,只用Na2CO3溶液就能将三种溶液区分开来的是( )
A.CuSO4、H2SO4、NaNO3 B.NaCl、CaCl2、Ba(NO3)2
C.HNO3、H2SO4、NaHCO3 D.HNO3、BaCl2、Na2SO4
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试(广东深圳卷)化学(解析版) 题型:探究题
如图为为实验室常用的实验装置,请回答问题

(1)写出装置的名称:a___ ___, b__ ____
(2)组装装置完毕,装药前要 ;若用AC装置组合制取氧气,实验中观察到水槽中气泡 时,开始收集,写出用高锰酸钾制取氧气的化学反应方程式:
(3)二氧化硫是一种具有污染性的气体,实验室用亚硫酸钠固体和浓硫酸来制取,则进行该反应所选用的发生装置是 (填字母),收集二氧化硫选用的是 装置,因此可知二氧化硫的密度 (填“大于”、“小于”或“等于”)空气的密度,F装置中的氢氧化钠溶液是足量的,原因是 (用方程式表示)
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试(山东省聊城卷)化学(解析版) 题型:选择题
下图为某医用葡萄糖注射液标签的一部分,据此下列说法不正确的是( )

A.该葡萄糖注射液中溶质的质量分数为5%
B.葡萄糖的相对分子质量为180
C.葡萄糖中碳元素、氢元素和氧元素的质量比为1:2:1
D.在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com