
| A. | K+ Na+NO3- CO32- | B. | Cu2+ Na+ NO3-SO42- | ||
| C. | Mg2+NH4+ NO3- Cl- | D. | Na+ Ba2+ Cl- SO42- |
分析 pH为1的水溶液显酸性,水溶液中含有大量的H+;根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存;本题还要注意能得到无色溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为1的水溶液显酸性,水溶液中含有大量的H+.
A、氢离子和碳酸根离子在溶液中相互交换成分生成水和二氧化碳,不能大量共存,故选项错误;
B、四者之间不反应,且能在酸性溶液中共存,但铜离子为蓝色,故选项错误;
C、四者之间不反应,且能在酸性溶液中共存,故选项正确;
D、钡离子和硫酸根离子在溶液中相互交换成分生成不溶于酸的硫酸钡沉淀,不能大量共存,故选项错误;
故选:C.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意在酸性溶液中共存.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:选择题
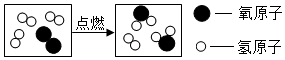
| A. | 该反应有单质生成 | |
| B. | 分子是化学变化中的最小粒子 | |
| C. | 如图表示的微观变化过程中共有三种分子 | |
| D. | 实际参加反应的“ ”分子与“ ”分子与“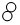 ”分子的个数比为1:3 ”分子的个数比为1:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 小科为研究质量守恒定律,把盛有5g16%的NaOH溶液的短试管放入盛有10g16%的CuSO4溶液的锥形瓶里,如图所示.倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是( )
小科为研究质量守恒定律,把盛有5g16%的NaOH溶液的短试管放入盛有10g16%的CuSO4溶液的锥形瓶里,如图所示.倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是( )| A. | 产生蓝色沉淀0.98g | |
| B. | 所得溶液的Na2SO4质量分数大于9.5% | |
| C. | 锥形瓶内物质总质量不变 | |
| D. | 所得的Na2SO4溶液质量与原CuSO4溶液质量相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

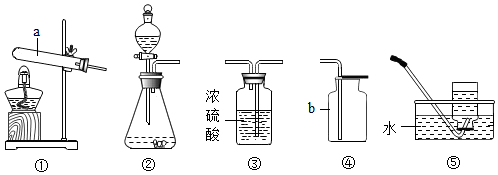
| 实验操作 | 实验现象 | |
| 甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热. | 黑色固体燃烧,发出红光,b中溶液变浑浊. |
| 乙组 | 取少量该黑色固体于a中,通入氧气(或O2),点燃酒精灯加热. | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊. |
| 实验次数 | 高蜡烛燃烧的时间 | 矮蜡烛燃烧的时间 |
| 第一次 | 23秒18 | 26秒06 |
| 第二次 | 23秒19 | 24秒94 |
| 第三次 | 20秒02 | 21秒45 |
| 第四次 | 15秒16 | 19秒10 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 海洋为人类提供了宝贵的自然资源.
海洋为人类提供了宝贵的自然资源.| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶解度/g | 36.0 | 21.6 | 37.2 | 9.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com