
某校课外小组同学将含有泥沙和碳酸钠杂质的食盐样品进行了如下实验:向一只60 g的烧杯中加入140 g样品,然后分5次加入盐酸,每次加入盐酸70 g(不考虑水、氯化氢逸出),每次反应完全后,称量烧杯和烧杯内物质的总质量。记录实验数据如下:
|
加入稀盐酸次数 |
1 |
2 |
3 |
4 |
5 |
|
烧杯和烧杯内物质的总质量/g |
267.8 |
335.6 |
403.4 |
471.2 |
541.2 |
第5次加酸后,烧杯底部剩余不溶固体1.8 g。已知泥沙成分为SiO2,它不溶于水,也不与盐酸发生反应。
请回答下列问题:
(1)反应过程中产生二氧化碳的总质量为 。
(2)食盐样品中钠元素与氯元素的质量比是多少?
(3)将实验后的溶液全部转化为氯化钠溶液,还需要加入碳酸钠粉末的质量是多少?
(1)8.8 g (2)食盐样品中钠元素与氯元素的质量比是276:355。
(3)5.3 g
【解析】(1)根据表格中所给数据可知,当加盐酸到第五次之后,物质的质量不在发生变化,说明此时样品全部反应,生成的二氧化碳质量也恒定不变.
(2)根据化学方程式,已知二氧化碳的质量可求出碳酸钠的质量,从而求出氯化钠的质量,样品中钠元素的质量为氯化钠与碳酸钠中钠元素质量之和,氯元素质量为氯化钠中氯元素质量
解:设食盐样品中碳酸钠的质量为x。
Na2CO3 + 2HCl ==== 2NaCl + CO2↑ + H2O
106 44
x 8.8 g
解得:x = 21.2 g
食盐样品中Na元素的质量:Cl元素的质量
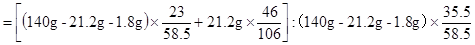
=276:355(或55.2 :71)
(3)分析表中数据,每70g盐酸与碳酸钠反应产生2.2g二氧化碳,第五次加入盐酸后盐酸没参加反应,因此剩余溶液中有70g稀盐酸没反应,根据二氧化碳的质量可求出所需碳酸钠的质量
解:设还需要碳酸钠粉末的质量为y。
Na2CO3 + 2HCl ==== 2NaCl + CO2↑ + H2O
106 44
y 2.2 g
解得:y=5.3 g
答:还需要碳酸钠粉末5.3 g。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
(2011年山东潍坊,26题)钢铁的生产和使用是人类文明和社会进步的一个重要的标志。
(1)每年钢铁锈蚀都会造成巨大的损失,铁制品锈蚀的主要原因是
。
(2)校课外兴趣小组的同学们去潍坊某钢铁长生铁样品进行实验:将四份不同质量的生铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表(已知:在标准状况下,22.4LH2的质量为2g)
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量 / g | 2.88 | 5.76 | 9.24 | 10.28 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
通过计算回答下列问题:
①上述表格中m的值为 。
②根据表中数据计算稀硫酸中H2SO4的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
(2011年山东潍坊,26题)钢铁的生产和使用是人类文明和社会进步的一个重要的标志。
(1)每年钢铁锈蚀都会造成巨大的损失,铁制品锈蚀的主要原因是
。
(2) 校课外兴趣小组的同学们去潍坊某钢铁长生铁样品进行实验:将四份不同质量的生
铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表(已知:在标准状况下,22.4LH2的质量为2g)
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量 / g | 2.88 | 5.76 | 9.24 | 10.28 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
通过计算回答下列问题:
①上述表格中m的值为 。
②根据表中数据计算稀硫酸中H2SO4的质量分数。
查看答案和解析>>
科目:初中化学 来源:2011年初中毕业升学考试(山东潍坊卷)化学 题型:计算题
(8分)钢铁的生产和使用是人类文明和社会进步的一个重要的标志。
(1)每年钢铁锈蚀都会造成巨大的损失,铁制品锈蚀的主要原因是
。
校课外兴趣小组的同学们去潍坊某钢铁长生铁样品进行实验:将四份不同质量的生铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的稀硫酸中,充分反应后,测得的实验数据如下表(已知:在标准状况下,22.4LH2的质量为2g)
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量 / g | 2.88 | 5.76 | 9.24 | 10.28 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com