
 图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t3℃时,将20 g乙加人50 g水中充分搅拌,可得到70 g溶液 | |
| C. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等 | |
| D. | 将t1℃甲、乙的饱和溶液各升温至t2℃,溶质质量分数相等 |
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;甲的溶解度大于乙的溶解度错误,因为没有指明温度;t3℃时,乙的溶解度是20g,将20g乙加人50g水中充分搅拌,可得到溶液的质量=10g+50g=60g,得到70g溶液不正确;t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等正确;将t1℃甲、乙的饱和溶液各升温至t2℃,溶质质量分数相等错误,还是乙大于甲.
解答 解:A、甲的溶解度大于乙的溶解度错误,因为没有指明温度;故选项错误;
B、t3℃时,乙的溶解度是20g,将20g乙加人50g水中充分搅拌,可得到溶液的质量=10g+50g=60g,得到70g溶液不正确,故选项错误;
C、由溶解度曲线可知:t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等,故选项正确;
D、将t1℃甲、乙的饱和溶液各升温至t2℃,溶质质量分数相等错误,还是乙大于甲,故选项错误;
故选C
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
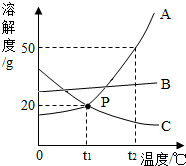 图是A、B、C三种物质的溶解度曲线.据图回答:
图是A、B、C三种物质的溶解度曲线.据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”表示氢原子,图“
”表示氢原子,图“ ”表示氧原子)
”表示氧原子)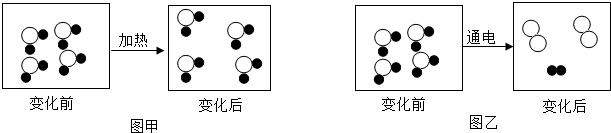
 ”微粒.
”微粒.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 茶氨酸由碳、氢、氧、氮四种原子构成 | |
| B. | 茶氨酸属于有机物,锌、硒指单质 | |
| C. | 茶氨酸中碳、氢、氧、氮四种元素的质量比是7:14:3:2 | |
| D. | 茶氨酸的化学式量是174 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com