��2013?���ݣ�ʵ�鴴������ѧ����Ϊ��Ҫ�Ŀ�ѧ��������ͼ��ijѧУʦ���ԡ�MnO
2��H
2O
2�ֽ�ʵ��װ�õĴ�����ơ���ʵ��������£�
�ٽ�һ֧���θ����ˮƽ���ã��õι���ȡ3ml���ܶ�Ϊlg/ml����������Ϊ5%��H
2O
2�������ܵ������ڣ�����ҩ��ȡ0.2gMnO
2��ĩ�����ڸ���Ľ����ܵĹܱ��ϣ�
�ڵ�ȼ�����Ϲ̶��İ������������ܲ������������۲�����
������ش𣺣�1���ɹ۲�������ǵİ�������
��ȼ
��ȼ
��
��2��д������ʵ����H
2O
2�ֽ�Ļ�ѧ��Ӧ����ʽ
��
��3���ٶ�����ʵ���е�H
2O
2��ȫ��Ӧ���ɲ�������������Ϊ
0.07
0.07
g������ȷ��0.01��
��4�����и�����ͬѧ�ǶԸô���ʵ������ۣ�����Ϊ���۲���������
BC
BC
��������ţ�
A��ʵ�������õ����������ϼ�ҩƷ���õ�
B��ʵ��ʹ�õ�ҩƷ����̫��
C����Ӧ�ٶ�̫��������ʱ��
D��ʵ���������ԣ�����װ�ú��Ƶ�ȼ�ĵ�����Ȥζ��ǿ





 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
 ��2013?���ݣ�����ͼ��ʾ����ȼ�ס�����֧����ȼ��һ���Ϩ�����ڿ���������ȼ�գ���һʵ��˵��ȼ�յ�����֮һ�ǣ�������
��2013?���ݣ�����ͼ��ʾ����ȼ�ס�����֧����ȼ��һ���Ϩ�����ڿ���������ȼ�գ���һʵ��˵��ȼ�յ�����֮һ�ǣ�������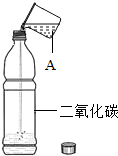 ��2013?���ݣ���ͼ�ǽ̲��С�������̼���ܽ���ʵ�顱--��һ���ռ���������̼������ʵؽ���������ƿ�м���Լ
��2013?���ݣ���ͼ�ǽ̲��С�������̼���ܽ���ʵ�顱--��һ���ռ���������̼������ʵؽ���������ƿ�м���Լ