


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
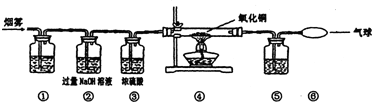
 (2006?贵阳)在实验室制取气体的实验中:
(2006?贵阳)在实验室制取气体的实验中:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2006?贵阳)金属是一类重要的材料,人类生产、生活都离不开金属.下面是小明同学对铁的部分知识的学习、探究.
(2006?贵阳)金属是一类重要的材料,人类生产、生活都离不开金属.下面是小明同学对铁的部分知识的学习、探究.
| ||
| ||
| 调查内容 | 脱漆的自行车 | 炒菜的铁锅 | 涂油的无锈铁钉 |
| 铁制品锈蚀的现象 | 风吹雨淋,时间长了脱漆处会生锈 | 清洗后,水擦干不易生锈,水未擦干易生锈 | 较长时间仍不生锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com