经分析某生石灰干燥已部分变质,取18g此干燥剂放入烧杯中,加入150g14.6%的稀盐酸充分反应,产生2.2gCO2,再继续加入过量的碳酸钙粉末,充分搅拌至不再产生气泡为止.产生2.2gCO2,过滤后,向滤液中加入164.4g水,计算此时溶液中溶质的质量分数.
解:根据氯元素守恒,无论经多少环节,最终氯元素要和钙元素结合成为最后的溶质.
设生成氯化钙的质量为x,加入的碳酸钙粉末中被消耗的碳酸钙的质量为y.
CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑
73 111
150g×14.6% x
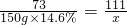
x=33.3g
CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑
100 44
y 2.2g
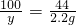
y=5g
溶液的质量=18g+150g+5g+164.4g-2.2g-2.2g=330.8g
溶液中氯化钙的溶质质量分数=
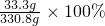
=10%
答:溶液中溶质的质量分数为10%.
分析:生石灰易吸收水分而变质,生成熟石灰,与稀盐酸反应都能生成氯化钙,碳酸钙与稀盐酸反应也能生成氯化钙,根据参加反应的盐酸的质量,求得生成的氯化钙的质量,进而求出溶液中溶质的质量分数.
点评:此题看似繁琐,实际上理解了就比较简单了,用氢氧化钙或生石灰或碳酸钙与盐酸反应的化学方程式进行计算都可,最终求出生成的氯化钙的质量即可.

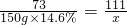
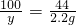
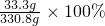 =10%
=10%