
| 组合序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 组合物质 | H2SO4 Ba(NO3)2 | H2SO4 NaOH | H2SO4 K2CO3 | Ba(NO3)2 NaOH | Ba(NO3)2 K2CO3 | ______ K2CO3 |


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
| 组合序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 组合物质 | H2SO4 Ba(NO3)2 |
H2SO4 NaOH |
H2SO4 K2CO3 | Ba(NO3)2 NaOH | Ba(NO3)2 K2CO3 | NaOH NaOH K2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 | 实验结论 |
取少量配置好的硫酸溶液,加入过量的硝酸钡溶液,充分振荡后过滤. 取少量配置好的硫酸溶液,加入过量的硝酸钡溶液,充分振荡后过滤. |
生成沉淀 生成沉淀 |
|
向过滤所得的滤液中滴加硝酸银溶液,振荡 向过滤所得的滤液中滴加硝酸银溶液,振荡 |
生成白色沉淀 生成白色沉淀 |
该溶液中含有氯离子 该溶液中含有氯离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
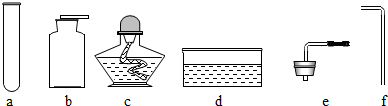
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com