
(13分)某兴趣小组利用下列装置进行O2、CO2 的实验室制法和有关性质的研究.
(1)写出下列编号仪器的名称:①________②________.
(2)甲同学要用高锰酸钾来制取O2, 应选用右图中的_________装置(填编号),该反应的化学方程式是:____________.当O2收集满并取出集气瓶后,停止该实验的正确操作的先后顺序为_____________.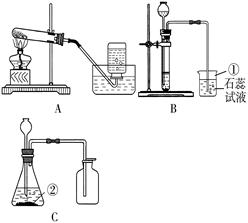
(3)查阅资料知:浓盐酸具有挥发性,能挥发出氯化氢.
①乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质时观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释有_____(填序号).
A.产生的CO2直接使石蕊试液变红
B.产生的CO2与水反应生成H2CO3使石蕊试液变红
C.挥发出的氯化氢溶于水使石蕊试液变红
②乙同学将制得的气体通入澄清的石灰水中,石灰水没有变浑浊,其原因是____________.
(4)丙同学用C装置制取了一瓶无色、无味的气体(纯净物),你推测该气体可能是___________,试用最简便的方法证实你的推测_________________________________.
(5)丁同学用下图所示装置完成一系列的实验.用实验装置的序号回答下列问题(尾气处理装置未给出).资料:白色的硫酸铜粉末遇水变成蓝色.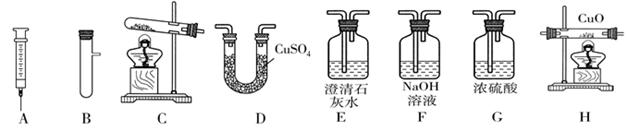
①实验室用仪器A、B可组合成制取氧气的反应装置,则发生反应的化学方程式为_______.
②检验CO中混有的CO2的装置是_______,除去CO中较多的CO2,最好选装置______.
③水煤气含有CO、H2、CO2、H2O.证明水煤气中含有CO和H2的实验装置的连接顺序是→
( )→( )→( )→( )→( )→尾气处理(从D~H中选择).
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2(2 Na2CO3?3 H2O2 )=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解;Ⅰ、制备研究:如图1是制备过碳酸钠的工艺流程.  请回答问题: (1)反应器中发生反应的化学方程式为 2Na2CO3+3H2O2═2Na2CO3?3H2O2 2Na2CO3+3H2O2═2Na2CO3?3H2O2 ;(2)生产中,反应及干燥均需在较低温度下进行,原因是 防止过碳酸钠分解,影响产量和产率 防止过碳酸钠分解,影响产量和产率 ;(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为 过碳酸钠在NaCl溶液中溶解度较小,易析出晶体 过碳酸钠在NaCl溶液中溶解度较小,易析出晶体 .(4)操作A的名称是 过滤 过滤 ,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒 玻璃棒 和漏斗 漏斗 ;(5)洗涤过碳酸钠晶体最好选用 B B .A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液 (6)母液可以循环使用,其中主要含有的溶质是 NaCl NaCl 和Na2CO3(或H2O2) Na2CO3(或H2O2) ;Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数. 小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验. [实验步骤]:① 检查气密性 检查气密性 ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中不再产生气体 不再产生气体 时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.[实验分析及数据处理]: (7)完善实验步骤的相关内容:① 检查气密性 检查气密性 、④不再产生气体 不再产生气体 ;(8)实验中,水的作用是 溶解过碳酸钠,利于其分解 溶解过碳酸钠,利于其分解 ;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是MnO2(或CuO) MnO2(或CuO) (填化学式);(9)实验中, A A ,则开始收集气体;A.刚开始出现气泡时 B.当气泡均匀连续出现时 C.若用带火星木条放在导管口部,复燃时 (10)若量筒中收集到气体的体积是224mL(通常情况下,氧气的密度近似为1.43g?L-1.),计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr(2Na2CO3?3H2O2)=314、Mr(O2)=32] 95% 95% ;[实验反思]: (11)经过讨论,小组同学一致认为测定结果偏大,可能原因是 滴入的水占据了锥形瓶内的体积,使得O2体积偏大 滴入的水占据了锥形瓶内的体积,使得O2体积偏大 ;(12)量筒中长导管的作用是 起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸) 起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸) ;(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由. 不正确,装置中原有空气和生成的O2等体积代换 不正确,装置中原有空气和生成的O2等体积代换 ;(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为 93.6% 93.6% .(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数? 想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定 想方法测出过碳酸钠和酸反应生成CO2的体积或质量,进而进行计算(或过碳酸钠和氯化钙、氯化钡等溶液生成沉淀质量进行测定 .(只需给出简要的方案)
查看答案和解析>> 科目:初中化学 来源:2011-2012年广东省潮州市凤洲中学九年级下学期月考化学试卷(带解析) 题型:探究题 (13分)某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。(本题的所有夹持仪器均已省略)请根据下图回答问题: 查看答案和解析>> 科目:初中化学 来源:2012届江苏省江阴初级中学九年级5月中考模拟化学试卷(带解析) 题型:探究题 (9分)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
⑸某同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该同学根据实验现象: ,判断NaOH溶液与稀盐酸发生了中和反应。 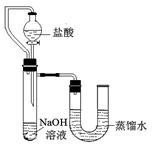 II、实验中的意外情况 在实验过程中,他们发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH和Na2CO3。 ⑹小明同学取白色粉末少许,溶于水后,先向溶液中加入足量的 溶液,看到白色沉淀产生,然后向上层清液中加入酚酞试液,看到溶液呈红色,验证了猜想③是正确的。 ⑺为了进一步研究,三位同学取了10.0g上述样品,利用电子天平共同做了下图所示的实验。  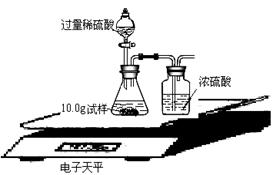 实验数据记录如下:
(8)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是(实验操作均正确): 。 查看答案和解析>> 科目:初中化学 来源:2011-2012年广东省潮州市九年级下学期月考化学试卷(解析版) 题型:探究题 (13分)某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。(本题的所有夹持仪器均已省略)请根据下图回答问题:
(1)图中仪器④⑤的名称:④ ,⑤ 。 (2)实验室制取氧气,某同学设计了图A的装置,并用仪器③收集氧气。其中,仪器①中盛放的试剂应为 ,此法生成氧气的化学方程式为 ,收集氧气的方法为 。用仪器③收集氧气时,还可用于测定氧气的体积, 此时还需要 (填仪器名称)。 (3)实验室制取二氧化碳,从B~G中选择仪器,组装发生装置,要求能方便控制反应的发生或停止,你的正确选择为(填字母) 。 (4)实验前,甲同学先向仪器①中加入水,然后将导管放人水槽中,并打开仪器①的活塞,观察导管口是否有连续的气泡出现。该实验操作的目的是__________。 (5)乙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2 ,实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究: 【提出猜想】猜想l:反应生成的MnO2分解放出O2; 猜想Ⅱ:反应生成的K2MnO4分解放出O2 做出上述猜想的理由是_______________________________。 【实验验证】同学们分为两组,分别进行以下实验: ①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想________________错误。 ②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是_________________ 。
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |