
【题目】晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据记录如表所示: 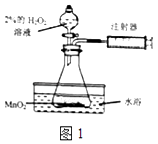
实验1 | 实验2 | |
MnO2的质量/克 | 0.5 | 0.5 |
2%的H2O2的体积/毫升 | 20 | X |
温度/℃ | 20 | 80 |
(1)实验2中X的值应为毫升;
(2)实验中,可通过来比较H2O2分解速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因是 . a、锥形瓶内气体受热膨胀 b、收集到的氧气中混有空气
c、温度较高时水蒸发成水蒸气 d、生成更多的氧气
(4)晓晓从家中拿来一瓶久置的医用过氧化氢溶液来测定该溶液中溶质质量分数.她取出该溶液51 g,加入适量二氧化锰,生成O2的质量与反应时间的关系如图2所示. 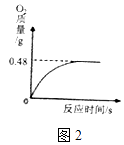
Ⅰ、完全反应后生成氧气的质量为moL.
Ⅱ、计算参与反应的过氧化氢的物质的量 .
Ⅲ、这瓶过氧化氢溶液的质量分数为 .
【答案】
(1)40
(2)相同的时间内注射器内气体的体积
(3)ac
(4)0.015;0.03mol;2%
【解析】解:(1)利用对比试验探究温度对H2O2分解反应速率的影响时,变量应是温度,其余的量应相同,所以,实验2中应加入5%H2O240毫升;(2)在两次实验中,可通过相同的时间内注射器内气体的体积来比较H2O2分解反应速率的大小;(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有温度较高时水蒸发成水蒸气;(4)Ⅰ、完全反应后生成氧气的质量为0.48g,物质的量为 ![]() =0.015mol 所以答案是:0.015mol;
=0.015mol 所以答案是:0.015mol;
Ⅱ、设参与反应的H2O2的质量为x,
2H2O2 |
| 2H2O+ | O2↑ |
68 | 32 | ||
x | 0.48g |
![]()
解得:x=1.02g
参与反应的过氧化氢的物质的量为: ![]() =0.03mol.
=0.03mol.
答:该过氧化氢溶液中过氧化氢的物质的量为0.03mol.
Ⅲ、这瓶过氧化氢溶液的质量分数 ![]() =2%.
=2%.
所以答案是:(1)40;(2)相同的时间内注射器内气体的体积;(3)ac;(4)0.015;0.03mol;2%.
【考点精析】认真审题,首先需要了解质量守恒定律及其应用(①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏).


科目:初中化学 来源: 题型:
【题目】化学就在我们身边.
(1)活性炭去除冰箱中的异味,是利用了它的性.
(2)生理盐水中的溶质是(填化学式).
(3)炒菜时油锅着火用锅盖盖灭,其灭火原理是
(4)打开汽水瓶盖,发现有大量气泡溢出,这种现象说明气体的溶解度与有关.
(5)家用燃料天然气的主要成分是甲烷,写出其燃烧的化学方程式 .
(6)高碳酸钾(K2FeO4)是一种新型高效的水处理剂,K2FeO4由种元素组成,1 moLK2FeO4中约含有钾原子个(用科学记数法表示).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活处处联系化学,下列说法不正确的是( )
A.稀有气体通电时发出五颜六色的光,这是利用其物理性质
B.厨房煤气管道漏气,立即关闭阀门并开窗通风
C.用甲醛浸泡保存海产品来保鲜
D.利用乳化原理使用洗洁精洗涤餐具上的油污
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂欲从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下: 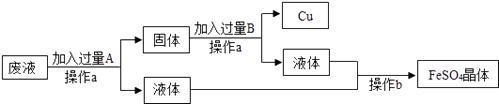
请回答下列问题:
(1)操作a的名称是
(2)写出流程中有关反应的化学方程式: . 以上两个反应能够发生的原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com