
【题目】通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解。现有H、N、O、Ca四种元素,请选用其中的元素写出下列物质的化学式:
①空气中含量最多的气体 ; ②改良酸性土壤的碱 ;
③含氧量最高的氧化物 ;④可作氮肥的盐 :
科目:初中化学 来源: 题型:
【题目】(1)用化学符号表示:
①1个铁原子 ;②空气中含量最多的物质 ;
③2个二氧化碳分子分子 ;④地壳中含量最多的金属元素 ;
⑤表示出二个硫酸根离子 ;⑥水中氧元素的化合价 ;
(2)写出下列反应的化学方程式,并在括号里注明反应的基本类型:
①铁在氧气中燃烧 ( )
②实验室用高锰酸钾制氧气 ( )
③金属钠与水反应生成氢氧化钠和氢气 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图1、图2所示装置,结合所学知识回答下列问题。
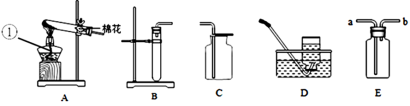
图1
(1) 图1中标号仪器的名称:①______________。
(2) 实验室用A装置制取氧气,写出反应的文字表达式__________________________,D装置收集满氧 气,并将集气瓶移出水面,___________(填“正放”或“倒放”)在桌面上。除了可以用D装置收集氧气,还可以选择图2装置中的___________进行收集(填写字母符号)。
![]()
![]()
![]()
![]()
![]()
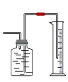
a b c d
图2
(3) 常温下二氧化硫(SO2)是一种无色有刺激性气味的气体,它的密度比空气大,能溶于水。实验室常用亚硫酸钠(Na2SO3)固体与稀盐酸在常温下反应制取SO2。制取SO2可从图1中选择的发生装置是 ,若用装置E收集SO2,则SO2应从 端通入(填“a”或“b”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列归纳和总结完全正确的一组是
A.对现象的认识 | B.对环境保护的认识 |
①打开盛有浓盐酸的瓶盖,瓶口出现白雾 ②氯化铵和熟石灰混合研磨,闻到刺激性气味 | ①二氧化硫排放过多会导致温室效应 ②生活污水的随意排放对水质有影响 |
C.对除杂的认识 | D.对性质和用途的认识 |
①用稀硫酸除去Zn中混有的Ag ②用灼烧的方法除去CuO中混有的C | ①石墨有良好的导电性,能作电极 ②银的导电性最好,可用作电线 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验课上,为检验镁条能否在N2中燃烧,某兴趣小组开展如下探究:
【查阅资料】氮化镁(Mg3N2)是一种淡黄色固体,能和水反应,生成Mg(OH)2和NH3;
【实验步骤】

①将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
②待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
③打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
④待钟罩内水面不再变化时,观察钟罩内壁及表面皿中固体颜色,取少量固体加入水中。
【分析】
(1)步骤①中足量白磷在钟罩内燃烧的目的是 ;
(2)步骤③中镁条剧烈燃烧,反应的化学方程式为 ;
(3)步骤④中钟罩内壁及表面皿中出现淡黄色固体,加入水中,产生白色浑浊及能使湿润红色石蕊试纸变蓝色的气体,反应的化学方程式为 ;
【结论】镁能在N2中燃烧,并生成Mg3N2。
(4)请你判断:2.40g镁条在某充满空气的密闭容器中完全燃烧,所得固体质量可能为 。
A.3.33g B.3.93g C.4.00g D.3.96g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气是一种宝贵的资源,下列关于空气各成分的说法正确的是
A. 空气中氮气的质量分数为78%
B. 填充稀有气体可以使灯泡经久耐用
C. 空气质量报告中所列的空气质量级别越大,空气质量越好
D. 氧气能支持燃烧,所以氧气具有可燃性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)在“水、氮气、稀有气体、明矾”中选择适当的物质填空:
①食品包装袋中防腐的气体是 ;②净化水时用作絮凝剂的是_ ;
③相对分子质量最小的氧化物是 ;④通电时发出不同颜色光的是_____ 。
(2)矿物质水中元素及国标含量如下表所示,请用化学符号填空

①矿物质水中含有的镁元素 ;
②久置的水中溶有一定量的氧气,请表示出2个氧分子 ;
③右表中的一种阴离子 ;
④氧化钙中钙元素的化合价为+2价 ;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】节约用水和合理开发利用水资源是每个公民应尽的责任和义务,你认为下列做法与之不相符的是( )
A.洗菜、洗衣、淘米的水用来浇花、拖地、冲厕所
B.将活性炭放入硬水中使其软化
C.生活污水要集中处理,以减少水体污染
D.加强工业废水的排放监控,坚持达标后排放
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究。
【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
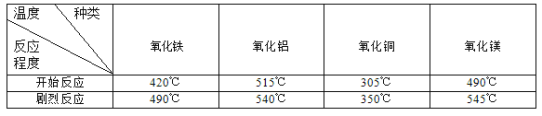
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是 。
【设计并完成实验】Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将X g氯酸钾与1.0g氧化铜均匀混合加热
【实验现象分析】Ⅲ中X的值应为 ,实验Ⅰ和Ⅲ比较可证明 。将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同,这些步骤是为了证明氧化铜在该化学反应前后 和 都不变。
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的符号表达式为 。
【实验反思】实验Ⅱ和Ⅲ对比的目的是 。
【提出问题】②MnO2的用量对 H2O2分解反应有何影响?
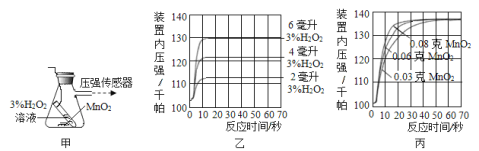
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计。)
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出 。
(2)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求。在此实验条件下,若MnO2的质量有4克(一药匙),就能使下图 (填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求。
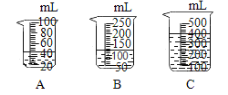
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com