
分析 (1)根据反应物接触越充分,反应进行的越快进行解答;
(2)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(3)根据过滤可以把不溶于水的物质除去进行解答;
(4)根据流程图可以判断那些物质可以循环利用.
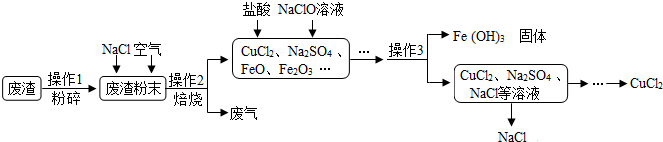
解答 解:(1)粉碎的目的是增大反应物的接触面积,提高了化学反应的速率;故填:大反应物的接触面积,提高了化学反应的速率;
(2)高温条件下,通入空气,CuS和NaCl反应生成了CuCl2和Na2SO4,化学方程式为:CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4;故填:CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4;
(3)操作3是过滤,通过过滤把不溶于水的物质和溶液分离,需要的玻璃仪器玻璃棒、烧杯、漏斗;故填:过滤;漏斗;
(4)流程图中能循环利用的物质是氯化钠.故填:氯化钠.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:初中化学 来源: 题型:实验探究题
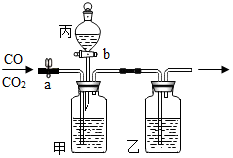 在实验室用如图所示装置进行CO和CO2的分离和干燥.现只有稀盐酸、浓硫酸、氢氧化钠溶液,按要求填写下列空白.
在实验室用如图所示装置进行CO和CO2的分离和干燥.现只有稀盐酸、浓硫酸、氢氧化钠溶液,按要求填写下列空白.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | NaOH溶液 | Na2CO3溶液 | 加入适量稀盐酸 |
| C | 铜粉 | 铁粉 | 加入过量的稀硫酸,过滤 |
| D | CaO | CaCO3 | 加水,溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
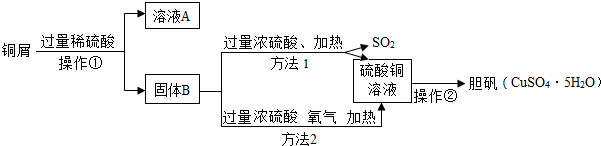
| A. | 操作①所用的玻璃仪器有烧杯、玻璃棒 | |
| B. | 铜屑表面呈绿色的物质俗称铜绿,化学式为Cu2(OH)2CO3 | |
| C. | 由固体B制取硫酸铜溶液的过程中,方法1更符合绿色化学要求 | |
| D. | 操作②的步骤为将硫酸铜溶液加热蒸干 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com