

分析 根据金属镁、铁、铜的性质以及金属活动性顺序进行分析,镁、铁、铜的金属活动性顺序为镁>铁>铜,且镁铁的活动性在氢前,所以使用磁铁分离出铁后,剩余的镁铜可通过与酸反应分离,也可通过镁与硫酸铜反应分离出铜,据此解决即可.
解答 解:(1)由于铁能被磁铁吸引,所以步骤Ⅰ中使用的物理方法是磁铁吸引,由题意可知要制取硫酸镁,镁能与硫酸反应,所以步骤Ⅱ中加入的试剂可以是硫酸溶液.
(2)由于铁的活动性大于铜,能将铜从其溶液中置换出来,所以利用金属A制得金属B是一种重要的冶金方法,例如:Fe+CuSO4═FeSO4+Cu.
故答为:(1)硫酸;(2)Fe+CuSO4═FeSO4+Cu.
点评 此题是一道实验探究物质分离的考查题,解题的关键是掌握物质的性质以及金属活动性顺序,属基础性知识考查题.


科目:初中化学 来源: 题型:填空题
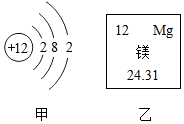 如图中,甲是镁原子的结构示意图,乙是镁元素在元素周期表中的相关信息.请回答:
如图中,甲是镁原子的结构示意图,乙是镁元素在元素周期表中的相关信息.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
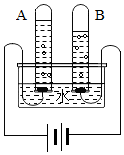 如图所示为电解水实验示意图,据图判断下列说法中正确的是( )
如图所示为电解水实验示意图,据图判断下列说法中正确的是( )| A. | 试管A中的气体能燃烧,发出淡蓝色的火焰 | |
| B. | 试管A和试管B中的气体体积比是2:1 | |
| C. | 该实验说明水是由氢气和氧气组成的 | |
| D. | 试管A中的气体是氧气,试管B中的气体是氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煤的直接燃烧会产生二氧化硫和氮的氧化物,可能导致酸雨 | |
| B. | 硝酸铵可用作复合肥,给植物提供所需的营养物质 | |
| C. | 做胃镜时不可以用碳酸钡代替硫酸钡作为钡餐使用 | |
| D. | 氯化钠是生活中常见的调味剂,高浓度的氯化钠溶液可以杀菌 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液是无色透明的,无色透明的液体不一定都是溶液 | |
| B. | 溶液体积等于溶质和溶剂体积之和 | |
| C. | 浓溶液是饱和溶液,饱和溶液不一定都是溶液 | |
| D. | 温度会影响固体溶解度大小,搅拌不会增大固体溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | (1)(2)(3) | B. | (2)(3)(4) | C. | (3)(4)(5) | D. | (1)(2)(4) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶液pH | 11.22 | 11.35 | 11.46 | 11.48 | 11.50 | 11.50 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com