
【题目】实验室常利用以下装置完成气体制备及性质实验。请回答:
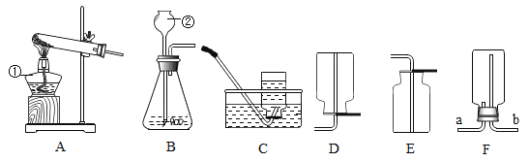
(1)指出编号仪器的名称:①_____②_____。
(2)以上_____(从A-E中选择)装置有一处明显的错误,请加以改正_____。利用改正后的装置继续完成后面的实验。
(3)用高锰酸钾制取氧气,应选择的发生装置是_____(填字母),为防止高锰酸钾粉末进入导管,应采取的措施是_____;请简述如何组装一套给试管里的固体加热的装置_____。
(4)在实验室制取二氧化碳气体,其反应原理用化学方程式表示为_____,将药品加入装置前,应先进行的操作是_____。若用F装置收集二氧化碳,验满的方法是_____。
【答案】酒精灯 长颈漏斗 A 导气管应露出橡皮塞少许即可 A 在试管口放一团棉花 先放置好酒精灯,然后根据酒精灯火焰的高度将盛有药品的试管固定在铁架台上,试管口略向下倾 2HCl+CaCO3=CaCl2+H2O+CO2↑ 检查装置的气密性, 把燃着的木条放在F装置中b端口,若木条熄灭,说明收集满了
【解析】
(1)由图中可知,①为酒精灯,②为长颈漏斗。
故填:酒精灯;长颈漏斗。
(2)由图中可知,A中试管内部的导管插入到试管太深,导气管应露出橡皮塞少许即可,其它装置未见明显错误,B中长颈漏斗应插入到液面以下,D、E收集气体时,导管都应插入到集气瓶底部,图中都没有问题。
故填:A;导气管应露出橡皮塞少许即可。
(3)高锰酸钾制取氧气的发生装置属于固体加热型,故应选择A装置,为防止高锰酸钾粉末进入导管,应在试管口放一团棉花,要组装一套给试管里的固体加热的装置,需先放置好酒精灯,然后根据酒精灯火焰的高度将盛有药品的试管固定在铁架台上,试管口略向下倾斜。
故填:A;在试管口放一团棉花;先放置好酒精灯,然后根据酒精灯火焰的高度将盛有药品的试管固定在铁架台上,试管口略向下倾斜。
(4)实验室制取二氧化碳气体的反应原理是用大理石或石灰石与稀盐酸反应,化学方程式为![]() ;任何有气体参加或是生成的反应,在药品加入装置前,都应先检查装置的气密性;二氧化碳的密度比空气大,用F装置收集二氧化碳时应a进b出,所以验满的方法是把燃着的木条放在F装置中b端口,若木条熄灭,说明收集满了。
;任何有气体参加或是生成的反应,在药品加入装置前,都应先检查装置的气密性;二氧化碳的密度比空气大,用F装置收集二氧化碳时应a进b出,所以验满的方法是把燃着的木条放在F装置中b端口,若木条熄灭,说明收集满了。
故填:![]() ;检查装置的气密性;把燃着的木条放在F装置中b端口,若木条熄灭,说明收集满了。
;检查装置的气密性;把燃着的木条放在F装置中b端口,若木条熄灭,说明收集满了。


科目:初中化学 来源: 题型:
【题目】根据图回答:
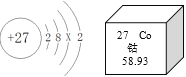
(1)钴原子的核电荷数是_____,X=_____。
(2)钴在化学反应中容易_____(填“得到”或“失去”)电子,相对原子质量是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将等质量的a、b两种固体,分别加入到盛有lO0g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是
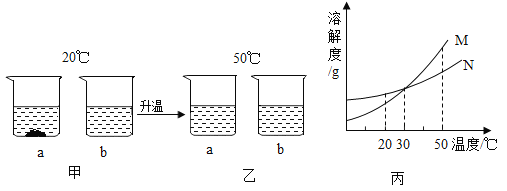
A.图丙中M表示b的溶解度曲线
B.图甲溶液中溶质的质量分数a大于b
C.图乙中a、b溶液一定是不饱和溶液
D.30℃时a、b溶液溶质质量分数不相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____)是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁(Mg2(OH)2CO3)和30%的过氧化氢溶液来制取过氧化镁。
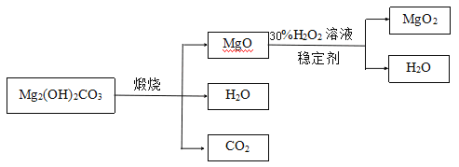
(资料)①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________(写出具体的操作和现象);上述生产过程加入稳定的剂的作用是________。
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________℃,煅烧的时间适宜控制在______h。
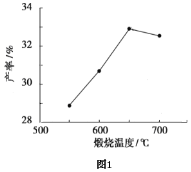
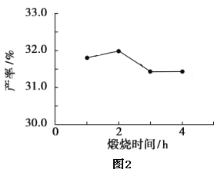
(5)结果在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。

①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________(写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】专家提醒:烧烤摊里会吃出“癌症风险”。腌制的肉串会产生一种叫做二甲基亚硝胺(C2H6N2O)的强致癌物质。请回答下列问题:
(1)该物质的相对分子质量为__________________________。
(2)该物质中碳元素和氮元素的质量比为_____________(答最简整数比)。
(3)3.7g该物质中氮元素的质量为______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在加热的条件下,Cu(NO3)2可分解为CuO、O2和某种氮的氧化物X,取一定质量的Cu(NO3)2固体充分加热,测得反应后生成CuO、O2、X的质量分别是8g、mg、9.2g。下列说法正确的是
A. m的值为1.6g
B. 氮的氧化物X的化学式是NO
C. 该反应方程式中,CuO和O2的化学计量数之比为3:2
D. 该反应只有一种元素化合价发生改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课本实验中,铁生锈需要较长的时间,某实验小组设计如下实验:
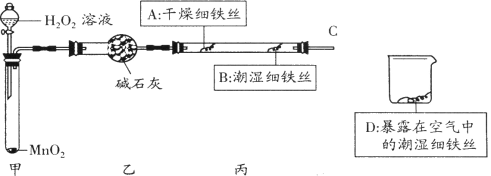
(1)写出甲试管中发生反应的化学方程式______;
(2)4分钟后观察:A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮。该实验说明铁生锈主要与______和______有关;
(3)B、D处实验现象对比说明:决定铁生锈快慢的一个重要因素是______;
(4)请写出日常生活中防止铁生锈的一种措施______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钾和碳酸钙的固体混合物 75g 与足量的稀盐酸充分反应后,如果将反应后的溶液蒸 干得到 82.7g 固体,则原混合物中金属元素的质量分数为( )
A. 40%B. 44%C. 48%D. 52%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纯碱(Na2CO3)是一种重要的有机化工原料。侯氏制碱法制出的纯碱常含少量NaCl杂质,化学兴趣小组对工业纯碱样品进行实验探究。
Ⅰ研究Na2CO3的性质
(1)Na2CO3溶液显____(填“酸性”、“中性”或“碱性”)。
(2)检验样品中碳酸根的方法是____。
Ⅱ设计以下实验方案,测定样品中Na2CO3的质量分数。
[方案一]取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。
(3)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为____。
(4)实验中判断沉淀是否完全的方法是____。
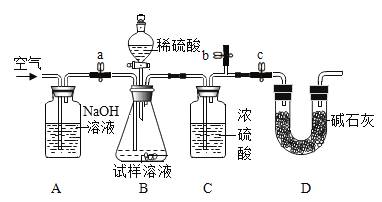
[方案二]采用如图装置,检查装置气密性;称取样品m1g于锥形瓶中,称装置D质量为m2 g;关闭止水夹c,打开止水夹a、b,缓慢鼓入空气数分钟,关闭止水夹a、b,打开止水夹c,缓慢加入稀硫酸至不再产生气体为止;打开止水夹a,缓慢鼓入空气数分钟,再称量装置D质量为m3g。
(查阅资料)浓硫酸具有吸水性,碱石灰的成分为CaO和NaOH固体
(5)装置B中发生的化学方程式为______。
(6)样品中Na2CO3的质量分数的计算式是______。
(7)反应后鼓入空气的目的是______。
(8)该测定结果比实际值偏高,从装置上分析其原因可能是______;改进措施为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com