【答案】
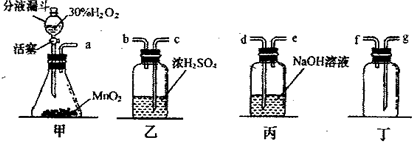
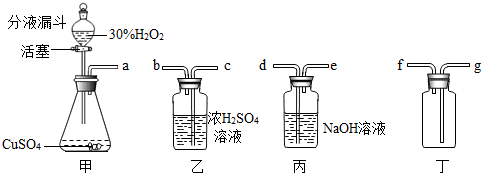
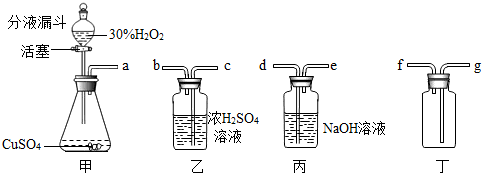
分析:(1)根据甲装置中的药品分析,写成制取氧气的化学方程式;
(2)根据氧气可以用浓硫酸干燥,并且可用向上排空气法收集分析解题;根据氧气验满的方法分析:将带火星的木条接近f口处,观察木条是否复燃;
(3)丁装置排水法收集气体时根据氧气不易溶于水,要“短进长出”分析;
(4)根据MnO
2是H
2O
2分解反应的催化剂,起到催化作用分析;根据物质的性质及混合物的分离方法分析;
(5)甲装置是固液反应制取气体的常见装置,可用来制取氧气、二氧化碳和氢气等.
解答:解:(1)甲装置中的过氧化氢溶液在二氧化锰的催化作用下,可以制取氧气,故反应的方程式为:2H
2O
2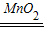
2H
2O+O
2↑;
(2)干燥氧气可用浓硫酸,导管长进短出,氧气的密度比空气大,所以氧气应从长导管进入,短导管排空气,所以装置的导管接口顺序为:a→c→b→g;检验氧气是否收集满用带火星的木条放于排空气的f口处,若木条复燃,说明收集满了;
(3)氧气不易溶于水,会聚集在水的上方,所以应从短管进,长管更易将水排尽,所以装置最合理的连接顺序为a→f;
(4)MnO
2是H
2O
2分解反应的催化剂,改变过氧化氢的分解速率;难溶性的固体和液体的分离可采用过滤的方法;
(5)甲装置是固液反应制取气体的常见装置,若只改变装置甲中的药品,此套装置还可以用来制取二氧化碳,因为二氧化碳的制取是大理石和稀盐酸的反应,反应的方程式为:CaCO
3+2HCl→CaCl
2+H
2O+CO
2↑;也可以是氢气的制取:Zn+H
2SO
4═ZnSO
4+H
2↑.
故答案为:CO
2(或H
2)(1分)
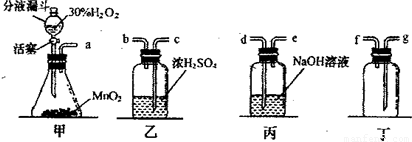
故答案为:(1)2H
2O
2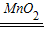
2H
2O+O
2↑;
(2)a→c→b→g;将带火星的木条放在f处,若复燃,则收集满;
(3)a→f;(4)催化剂;过滤;
(5)CO
2(或H
2);CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑(或Zn+H
2SO
4═ZnSO
4+H
2↑).
点评:了解过氧化氢制取氧气的原理及二氧化锰在反应中的作用,常用仪器的用途,氧气的验满方法,装置连接及物质的分离和提纯等知识是正确解答的关键.

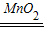 2H2O+O2↑;
2H2O+O2↑;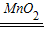 2H2O+O2↑;
2H2O+O2↑;