
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:初中化学 来源: 题型:
“蜂窝煤”比煤球更有利于煤的完全燃烧、提高燃烧效率,这主要是因为( )
A. 降低了煤的着火点 B. 升高了煤的着火点
C. 提高了氧气的浓度 D. 增大了煤与氧气的接触面积
查看答案和解析>>
科目:初中化学 来源: 题型:
在探究二氧化锰、氧化铜、氧化铁对过氧化氢溶液分解速率的影响的过程中,没有必要进行控制的变量是( )
A.过氧化氢溶液中溶质的质量分数 B.催化剂的质量
C.反应容器的形状 D.反应前过氧化氢溶液的温度
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学需测定某100g过氧化氢溶液中所含过氧化氢的质量。他取10g二氧化锰放入烧杯中,并将该过氧化氢溶液全部加入,不同时间用电子天平测量其质量,所得读数如下表所示:
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯及所盛物质总质量/g | 335.70 | 334.30 | 334.00 | 333.50 | 333.00 | 332.50 | 332.50 |
(1)试分析,100g过氧化氢溶液完全反应后生成氧气的质量为 。(2分)
(2)计算100g过氧化氢溶液中过氧化氢质量分数为多少?(写出计算过程)(6分)
(3)请分析该方法测定结果可能会偏大的原因有 (写出一点即可)(2分)
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学用量筒量取液体的体积,量筒放平稳并面对刻度线。初次仰视读数为19mL,倾倒出部分液体后,其俯视读数为10mL,则该学生实际倾倒出的液体体积是 ( )
A、9mL B、大于9mL C、小于9mL D、无法判断
查看答案和解析>>
科目:初中化学 来源: 题型:
从下图所示的实验仪器中,选择相关的实验仪器,按要求填写下列空白:
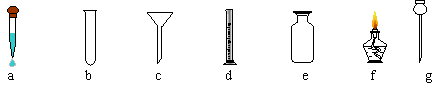 |
(1) a仪器的用途是 ,其名称是 ;
(2) 收集气体一定要用到的仪器是 (填编号),其名称是 ;
(3)g仪器的名称是 ,它的用途是 ;
(4)用于少量试剂间反应的仪器是 (填编号),其名称是 ;
查看答案和解析>>
科目:初中化学 来源: 题型:
如图为下册教材119~120页的二幅图,请据图判断下列叙述中错误的是( ) 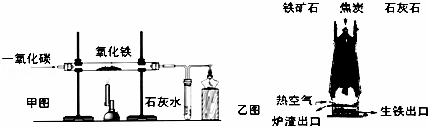
A. 甲图中炼铁时要注意先通一氧化碳后加热
B. 乙图中高炉炼铁时中原料焦炭的作用是:只产生热量
C. 乙图中生铁出口低于炉渣出口的原因是:生铁密度大于炉渣密度
D. 甲、乙图中得到产物的区别是:甲图中完全反应后得到纯净物,而乙则得到混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后, 得到了肯定的答案,邀请你一起对此展开探究。
得到了肯定的答案,邀请你一起对此展开探究。
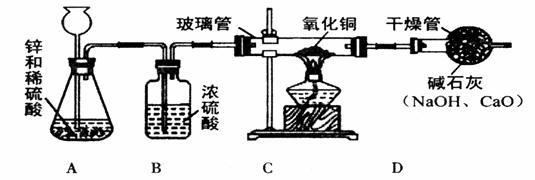
[设计方案]甲同学利用氢气还原氧化铜的原理和下图装置及药品进行实验(操作规范)。洗气瓶B中浓硫酸的作用为________________________
[实验探究]当玻璃管中固体由黑色转变为红色时,实验测得:
①装置C的玻璃管和其中固体的总质量在反应后减少了1.6g;
②装置D的干燥管和其中物质的总质量在反应后增加了1.82g,用此数据算得水中H、O元素的质量比为________,而由水的化学式算得H、O元素的质量比为________。
[分析交流]针对上述结果与理论值有偏差,乙同学认为:该装置存在缺陷,此观点得到了大家的认同,你对此改进的方法是________________________________________________ (假设生成的水完全被D中碱石灰吸收,装置内空气中的水蒸气、CO2忽略不计)。小组同学用改进后的装置重新实验得到了正确结果。
[意外发现]丙同学不小心将反应后的少量红色固体a洒落到足量稀硫酸中了,发现除了有红色固体b以外,溶液的颜色由无色变为蓝色。
[提出问题]铜与稀硫酸是不反应的,这里溶液的颜色为什么会变蓝呢? 
[查阅资料]
①CuO被还原的过程中会有Cu2O生成,Cu2O也能被还原在Cu;
②Cu2O固体是红色的,它一稀硫酸的反应为:Cu2O+H2SO4=CuSO4+Cu+H2O.
[得出结论]红色固体a中含有Cu2O。
[分析交流]红色固体a中含有Cu2O是否会影响水组成的测定结果________ (填“影响”或“不影响”)。
[提出猜想]针对红色固体a的成分,小组同学提出猜想①是:Cu2O和Cu;猜想②是:________。
[拓展探究]丁同学利用改进后的装置及药品重新实验, 通过测量反应前后固体质量的方法去确定哪种猜想成立,他已称得:①玻璃管的质量;②反应前红色固体a和玻璃管的总质量,完全反应后,你认为他还需要称量________的质量。
通过测量反应前后固体质量的方法去确定哪种猜想成立,他已称得:①玻璃管的质量;②反应前红色固体a和玻璃管的总质量,完全反应后,你认为他还需要称量________的质量。
[教师点拨]称取一定质量的红色固体a与足量的稀硫酸充分反应后,经过滤、洗涤、干燥后再称量红色固体b的质量,也可以确定哪种猜想成立。
[定量分析]小组同学再次实验,他们开始称取质量为3.6g的红色固体a,与足量的稀硫酸完全反应后得到红色固体b为2g。假如3.6g红色固体a都是Cu2O,请你计算出生成铜的质量(利用Cu2O+H2SO4=CuSO4+Cu+H2O.进行计算,写出计算过程);然后,通过与实际得到的固体2g进行比较,判断猜想________成立(填①或②)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com