
 如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:配制100g溶质质量分数为14.6%的稀盐酸,需用这种盐酸多少毫升,蒸馏水多少毫升?
如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:配制100g溶质质量分数为14.6%的稀盐酸,需用这种盐酸多少毫升,蒸馏水多少毫升?  名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 在反应中,Cr元素的化合价发生了变化 | |
| B. | 该反应有新原子产生 | |
| C. | 反应遵循质量守恒定律 | |
| D. | 反应生成的Cr2(SO4)3中Cr元素的化合价为+3价 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.同学们很感兴趣,决定对其成分进行探究.
化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.同学们很感兴趣,决定对其成分进行探究.| 实验 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| Ⅰ | 取样于试管中,向其中滴加无色酚酞. | 无色溶液变红色 | 该结论不可能是氯化钠 溶液.理由是氯化钠溶液不会使酚酞试液变红色. |
| Ⅱ | 另取样于另一支试管中,向其中滴加足量的稀盐酸. | 产生大量的气泡 | 该溶液中为碳酸钠.有关反应的化学方程式为:2HCl+Na2CO3=2NaCl+H2O+CO2↑. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
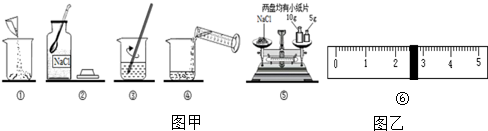
| 编号 | 0.25%淀粉溶液(ml) | 蒸馏水(ml) | 0.3%NaCl溶液(ml) | 1%CuSO4溶液(ml) | 唾液溶液(ml) | 加入碘液3滴后现象 |
| 1 | 3 | 2 | - | - | - | 变蓝色 |
| 2 | 3 | 1 | - | - | 1 | 不变蓝 |
| 3 | 3 | - | 1 | - | 1 | 不变蓝 |
| 4 | 3 | - | - | 1 | 1 | 变蓝色 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
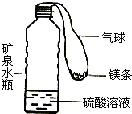 氢气曾被用于飞艇和载人气球.某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).矿泉水瓶和气球的质量为20g,气球中镁条的质量为4.8g,瓶中盛有溶质质量分数为30%的硫酸溶液75.2g,瓶底与桌面的接触面积为4cm2.(Mg+H2SO4═MgSO4+H2↑)
氢气曾被用于飞艇和载人气球.某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).矿泉水瓶和气球的质量为20g,气球中镁条的质量为4.8g,瓶中盛有溶质质量分数为30%的硫酸溶液75.2g,瓶底与桌面的接触面积为4cm2.(Mg+H2SO4═MgSO4+H2↑)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡. | 有气泡冒出. | 氢氧化钠溶液一定变质了. |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 有白色沉淀生成. | 说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色. | 说明原溶液中一定有氢氧化钠. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com