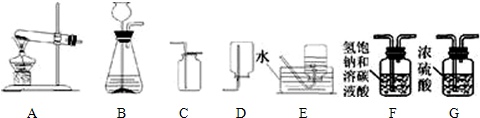
解:(1)实验室用加热氯酸钾或高锰酸钾制氧气属于固体加热制气体,故选A;用双氧水制取氧气属于固体和液体制气体,故选B;
用装置A制氧气,需要加热,可为氯酸钾或高锰酸钾的分解,故化学方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑或2KClO
3
2KCl+3O
2↑,若发生装置选B:2H
2O
2
2H
2O+O
2↑;
(2)明是“将二氧化锰加入装有过氧化氢溶液的锥形瓶中”,小亮是“把过氧化氢溶液缓缓加入盛有少量二氧化锰的锥形瓶中”,因此为得到平稳的气流,应采取小亮的做法,以达到通过控制药品加入而控制反应速度的目的;
(3)利用二氧化碳能使澄清石灰水变浑浊,使用澄清石灰水检验二氧化碳反应的化学方程式为CO
2+Ca(OH)
2=CaCO
3↓+H
2O;
(4)将气体通入新配制的饱和澄清石灰水中,始终未出现浑浊,由于石灰水是新制的,因此不可能是石灰水的原因,那么就只能是所通入气体的原因;在二氧化碳混入HCl气体时,能导致此现象的出现,利用HCl能与饱和碳酸氢钠溶液反应而二氧化碳不能,可选取把气体通过饱和的碳酸氢钠溶液除去混在二氧化碳中的HCl气体,再通入浓硫酸干燥,达到净化二氧化碳的目的,最后用向上排空气法收集.
故答案为:
(1)A(或B);若发生装置选A:2KMnO
4
K
2MnO
4+MnO
2+O
2↑或2KClO
3
2KCl+3O
2↑;
若发生装置选B:2H
2O
2
2H
2O+O
2↑;
(2)小亮;
(3)CaCO
3↓
(4)F; G; C.
分析:(1)根据实验室制氧气的反应原理选择发生装置;
(2)将二氧化锰加入装有过氧化氢溶液的锥形瓶中,反应速度不能得到控制;把过氧化氢溶液缓缓加入盛有少量二氧化锰的锥形瓶中,通过控制加入药品的速度达到控制反应速度的目的;
(3)检验二氧化碳通常采用澄清石灰水,澄清石灰水变浑浊则证明气体为二氧化碳;
(4)如果二氧化碳气体中混合HCl,则将气体通入新配制的饱和澄清石灰水中,也不能出现浑浊,此时可把气体通过饱和的碳酸氢钠溶液除去气体中的HCl,以达到净化二氧化碳气体的目的.
点评:掌握正确氧气的反应原理、装置和注意事项;了解检验和验满二氧化碳的方法,根据题意正确书写化学方程式.

 K2MnO4+MnO2+O2↑或2KClO3
K2MnO4+MnO2+O2↑或2KClO3 2KCl+3O2↑,若发生装置选B:2H2O2
2KCl+3O2↑,若发生装置选B:2H2O2 2H2O+O2↑;
2H2O+O2↑; K2MnO4+MnO2+O2↑或2KClO3
K2MnO4+MnO2+O2↑或2KClO3 2KCl+3O2↑;
2KCl+3O2↑; 2H2O+O2↑;
2H2O+O2↑; 

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案

