
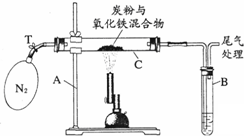
 某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:分析 (6)①根据题中所给化学方程式所需的条件进行分析使用酒精喷灯的原因.
②根据反应物与装置中空气的反应进行分析.
③根据二氧化碳的性质来分析.
④可直接根据化学方程式进行求解.
⑤根据质量守恒定律可知反应后获得气体的质量为前后玻璃管内物质的质量之差.
(7)根据③问计算的二氧化碳的质量和④问计算所得的气体的质量大小进行分析解答
解答 解:(1)①根据反应的反应条件为高温,可知选酒精喷灯是为了获得高温.故答案为:获得高温;
②因为反应物中碳可以在加热条件下可以和空气中的氧气发生反应生成二氧化碳,影响实验结果,所以目的就是清除试管中的空气.
故答案为:清除试管中空气(氧气),防止炭粉与空气中氧气发生反应;
③该试剂需将生成的二氧化碳完全吸收,故是碱溶液,故填:氢氧化钠溶液或足量的氢氧化钙溶液;
④设3.20gFe2O3与炭粉发生反应生成C02的质量为x
2Fe203+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3C02↑
320 132
3.2 g x
$\frac{320}{132}=\frac{3.2g}{x}$
解之得:x=1.32g
答:3.20g氧化铁完全反应时生成CO2的质量为1.32g;
故填:1.32 g;
⑤根据质量守恒定律可知:实验产物中气体质量为(48.48g+3.20g+2.00g)-52.24 g=1.44g;
故填:1.44 g;
(7)因为生成的气体质量为1.44 g>1.32 g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立;故填:因为生成的气体质量为1.44 g>1.32 g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立.
点评 本题主要是以实验探究兼计算题的形式,给出有关的信息提示和相关数据,让学生通过实验探究,及根据有关的化学方程式和该物质的组成成分,进行综合计算和判断.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:初中化学 来源: 题型:解答题
| OH- | NO3- | SO42- | Cl- | |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
| 金 属 | Ni | Zn | Cu |
| 与盐酸反 应的现象 | 气体产生缓慢, 金属逐渐溶解 | 气体产生迅速, 金属迅速溶解 | 无现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水槽、烧瓶、试管 | B. | 烧杯、蒸发皿、坩埚 | ||
| C. | 集气瓶、蒸发皿、烧瓶 | D. | 量筒、锥形瓶、漏斗 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气的化学性质比较活泼,它能与许多物质发生氧化反应 | |
| B. | 有氧气参加的化学反应不一定是化合反应 | |
| C. | 在一定条件下氧气可以变为无色液体 | |
| D. | 铁生锈是缓慢氧化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸溶液的pH越大,酸性越强 | |
| B. | 碱溶液的pH大于7,盐溶液的pH等于7 | |
| C. | 测定溶液的pH时,若将pH试纸湿润,测得的pH值将偏小 | |
| D. | “雪碧”等碳酸型饮料的pH小于7,晃动后打开瓶盖,其pH将变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com