
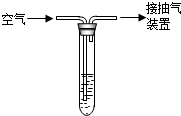
 硫或含硫物质在空气中燃烧生成SO2,SO2是一种无色、有刺激性气味的有毒气体.
硫或含硫物质在空气中燃烧生成SO2,SO2是一种无色、有刺激性气味的有毒气体.| 浓度限值(mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
| 2t | ||
|
| ||
| ||
| 64 |
| x |
| 254 |
| 1.27mg |
| ||
| ||


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(四川资阳卷)化学(解析版) 题型:推断题
含硫的物质在实验室或工业生产过程中可出现下列图示的转化:
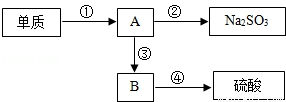
(1)实验室中,单质硫是 色固体,点燃少量单质硫于充满氧气的集气瓶中燃烧,产生漂亮的蓝紫色火焰,生成物质A.
(2)A是工业排放物中一种主要的空气污染物,也是酸雨形成的主因之一.根据你学过的知识可将A转化成Na2SO3,你提供的试剂是 溶液.
(3)在硫酸工业中,将A在一定条件下与空气中的物质反应得到B,B与水结合得到硫酸.B与A的组成元素相同,B中硫元素与硫酸中硫元素化合价相同,写出A转化成B的化学方程式: .实验室测定,B与水结合时温度升高,则反应④为 反应(选填“吸热”或“放热”).
(4)上述物质转化过程中,属于化合反应的是 (填序号).
(5)若回收工业排放物A 32吨,理论上可生产硫酸 吨.
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为________.实验完毕后,称得所得固体的质量小于4.0g.
小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为________.实验完毕后,称得所得固体的质量小于4.0g. C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2查看答案和解析>>
科目:初中化学 来源:2013年湖南省衡阳市中考化学试卷(解析版) 题型:填空题
 C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com