解:
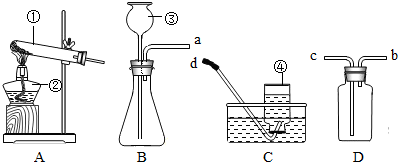
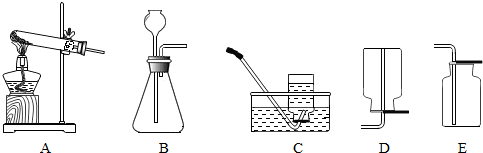
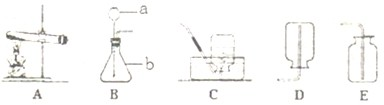
(1)A装置可以用来制取氧气,b装置可以用来制取氧气(过氧化氢做反应物)、氢气和二氧化碳.所以在实验室可用同一气体发生装置制取O
2、H
2、CO
2三种气体,指的就用B装置来制取.而用b装置来制取O
2的是应该是过氧化氢在二氧化锰的催化作用下实现的.
(2)实验室制取O
2、H
2、CO
2三种气体的反应:
A.需要加热:制取氧气若用高锰酸钾或者氯酸钾才需要加热,而用过氧化氢则不需要加热;氢气和二氧化碳的制取都不需要加热.所以不选.
B.需用催化剂:只有用氯酸钾或者过氧化氢制取氧气时才用到催化剂,高锰酸钾制取氧气无需催化剂;而氢气和二氧化碳的制取,不需要催化剂.所以不选.
C.没有气体参加反应:以上三种气体的反应物都没有气体.可选.
D.生成的气体只有一种:以上三种气体制取的反应中生成物只有一种气体.可选
故选CD.
(3)a.2NH
4Cl(固)+Ca(OH)
2(固)

CaCl
2+2NH
3↑+2H
2O,由于是固体在加热条件下制取氨气的,所以发生装置应该为A.
b.NH
4HCO
3(固)

NH
3↑+CO
2↑+H
2O,本反应生成物中有两种气体,导致产物不纯净,难以分离,所以不适合用来实验室制取气体.
c.CaO(固)+NH
3?H
2O=NH
3↑+Ca(OH)
2,是固体和液体在不加热的情况下来制取氨气,所以发生装置可以选B.由于氨气密度小于空气,且极易溶解于水,所以只能采用向下排空气法收集,收集NH
3应选择装置D.
故答案为:
(1)2H
2O
2
2H
2O+O
2↑ (2)CD;(3)A B 反应生成两种气体,产物不纯净 D
分析:实验室制取气体时,在原理选择上应该注意的是:1、制取气体的反应物不能是气体;2、生成物中只能有一种气体;3、要实验简便可行,实验要求和仪器要容易满足.
(1)在实验室可用同一气体发生装置制取O
2、H
2、CO
2三种气体,由于氢气制取是用液体和固体不加热来实现的,即为B装置,所以就是说可以共用的装置为B,而用B制取氧气时应该选用的原料为过氧化氢和二氧化锰.
(2)在实验室制取O
2、H
2、CO
2三种气体的反应中,氧气制取可以加热也可以用不加热的,而氢气制取不需要加热,二氧化碳制取不需要加热;在三种气体中只有氧气的制取可以用到催化剂.而实验室中制取这三种气体的原理都没有用到气体作为反应物,且生成物只有一种气体.
(3)a.2NH
4Cl(固)+Ca(OH)
2(固)

CaCl
2+2NH
3↑+2H
2O,这是固体在加热条件来制取气体的,所以发生装置应该为A.b.NH
4HCO
3(固)

NH
3↑+CO
2↑+H
2O,本反应中生成物含有两种气体,导致气体不纯净,也很难分离,所以不宜用来制取气体.c.CaO(固)+NH
3?H
2O=NH
3↑+Ca(OH)
2,是固体和液体在不加热条件下来制取氨气的,,所以可以选用B装置来作为发生装置.由于氨气极易溶解于水,所以不能用排水法收集.同时由于其密度小于空气,所以可采用向下排空气法收集.
点评:实验室制取气体时原料不能为气体,生成物也不能是多种气体,否则导致得到的气体不纯.

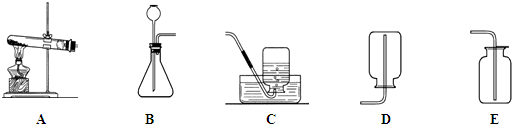
 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O CaCl2+2NH3↑+2H2O,由于是固体在加热条件下制取氨气的,所以发生装置应该为A.
CaCl2+2NH3↑+2H2O,由于是固体在加热条件下制取氨气的,所以发生装置应该为A. NH3↑+CO2↑+H2O,本反应生成物中有两种气体,导致产物不纯净,难以分离,所以不适合用来实验室制取气体.
NH3↑+CO2↑+H2O,本反应生成物中有两种气体,导致产物不纯净,难以分离,所以不适合用来实验室制取气体. 2H2O+O2↑ (2)CD;(3)A B 反应生成两种气体,产物不纯净 D
2H2O+O2↑ (2)CD;(3)A B 反应生成两种气体,产物不纯净 D CaCl2+2NH3↑+2H2O,这是固体在加热条件来制取气体的,所以发生装置应该为A.b.NH4HCO3(固)
CaCl2+2NH3↑+2H2O,这是固体在加热条件来制取气体的,所以发生装置应该为A.b.NH4HCO3(固) NH3↑+CO2↑+H2O,本反应中生成物含有两种气体,导致气体不纯净,也很难分离,所以不宜用来制取气体.c.CaO(固)+NH3?H2O=NH3↑+Ca(OH)2,是固体和液体在不加热条件下来制取氨气的,,所以可以选用B装置来作为发生装置.由于氨气极易溶解于水,所以不能用排水法收集.同时由于其密度小于空气,所以可采用向下排空气法收集.
NH3↑+CO2↑+H2O,本反应中生成物含有两种气体,导致气体不纯净,也很难分离,所以不宜用来制取气体.c.CaO(固)+NH3?H2O=NH3↑+Ca(OH)2,是固体和液体在不加热条件下来制取氨气的,,所以可以选用B装置来作为发生装置.由于氨气极易溶解于水,所以不能用排水法收集.同时由于其密度小于空气,所以可采用向下排空气法收集.