
 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).分析 (1)利用石蕊遇酸的变色情况分析即可;
(2)综合分析酸的化学性质可对A的类别进行判断;
(3)根据铁锈的成分结合与盐酸反应的产物对化学方程式书写即可;
(4)镁与盐酸反应生成氯化镁和氢气;
(5)酸与盐的反应一定要符合复分解反应的发生条件.
解答 解:(1)石蕊遇酸性溶液会变红色,所以将紫色石蕊试液滴加到盐酸溶液中溶液变红,故填:红
(2)综合分析酸的化学性质可知:除去盐酸能与指示剂、金属氧化物、金属、盐反应外还能与碱发生中和反应;
(3)铁锈的主要成分是氧化铁,与盐酸反应时会生成氯化铁与水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
(4)镁与盐酸反应生成氯化镁和氢气,化学方程式为:Mg+2HCl═MgCl2+H2↑;
(5)实验室用大理石和稀盐酸反应制取二氧化碳,可选择碳酸钙.
故答案为:(1)红;
(2)碱;
(3)Fe2O3+6HCl═2FeCl3+3H2O;
(4)Mg+2HCl═MgCl2+H2↑;
(5)碳酸钙.
点评 熟练掌握酸的化学性质与酸碱盐之间的反应规律是解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
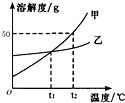
| A. | 要从甲的溶液中获得甲的晶体,可以采用降温结晶的方法 | |
| B. | 升高温度可以使甲的不饱和溶液变为饱和溶液 | |
| C. | t1℃时,甲、乙两种物质的饱和溶液中,溶质质量分数相等 | |
| D. | t1℃时,甲饱和溶液溶质质量分数为50% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Y>X>Z | B. | X>Y>Z | C. | Y>Z>X | D. | Z>Y>X |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com