
����Ŀ��KCl��KNO3���ܽ�ȱ����ܽ��������ͼ��ʾ������˵������ȷ���ǣ�������
�¶�/�� | 20 | 30 | 40 | 50 | |
�ܽ��S/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
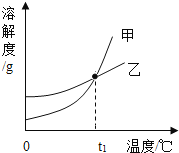
A. �ױ�ʾKNO3�ܽ������
B. �¶�t1��Ӧ��20��30��֮��
C. 40��ʱ��10gKC1����20gˮ�У��ɵõ�33.3%����Һ
D. 50��ʱ��30gKNO3����50gˮ������ܽ⣬�ٽ��µ�30�����о�������
���𰸡�C
��������
A��ͨ�������ܽ�ȱ��е����ݿ�֪������ص��ܽ�����¶ȱ仯Ӱ��ϴ����Լױ�ʾKNO3�ܽ�����ߣ���A��ȷ�����������⣻
B��20��30�棬�Ȼ��ص��ܽ�ȴ�34g����37g������ص��ܽ�ȴ�31.6g����45.8g�������¶�t1��Ӧ��20��30��֮�䣬��B��ȷ�����������⣻
C��40��ʱ���Ȼ��ص��ܽ����40.0g������10gKCl����20gˮ�У��й���ʣ�࣬�γɵ��Ǹ��¶��µ��Ȼ��ر�����Һ������Һ����������Ϊ��![]() ����C���������⡣
����C���������⡣
D��30��ʱ������ص��ܽ����45.8g������50��ʱ��30g KNO3����50gˮ������ܽ⣬�ٽ��µ�30�棬�о�����������D��ȷ�����������⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ȷ��ӳ��Ӧ�仯��ϵ����
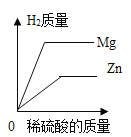
A. ��������þ��п�зֱ�����Ũ�ȵ�ϡH2SO4������
B. ��������CaO��Ca(OH)2�зֱ�����Ũ�ȵ�ϡ����������
C. CaCl2��HCl�Ļ����Һ�м���Na2CO3��Һ������
D. AgNO3��Cu(NO3)2�Ļ����Һ�м���п��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��һ�ֺ�ɫ����,������ϡ���ᡣijͬѧ��֪����ϡ�����е���������(H2O��H+��SO42-)��ʹ����ͭ�ܽ⡣�������һ��ͨ��ͼ��I��II��III����ʵ��������̽�����
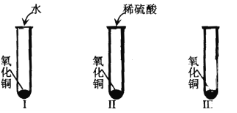
��1��������ļ����� ������������
��2��ͨ��ʵ��I����֤����������������������
��3��Ҫ֤���������������ܷ��ܽ�����ͭ������Ҫ����ʵ��II��III����III��Ӧ�ü�������������
��4��̽���Ľ��Ϊ ������Ϊ��ʵ��II��III���õ��Լ��⣬���ܹ��ܽ�����ͭ����һ�ֳ��������� ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Һ��˵���У���ȷ���ǣ� ��
A. �����½�10mL����Ca(OH)2��Һ���ȵ�50�棬��ʹ��Һ�ɱ�����Һ��Ϊ��������Һ
B. ��95gCaCl2��Һ���ɵõ�15g���壬��ԭ��Һ��CaCl2���ʷ���Ϊ15%
C. ����������Ϊ10%��H2SO4��Һ��ȡ��10mL����ȡ����10mLH2SO4��Һ���ʷ�����Ϊ10%
D. 20��ʱ��50gˮ���ܽ���18gNaCl����20��ʱNaCl���ܽ��Ϊ36g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ۺϴ����Ʊ�FeSO47H2O���������£�
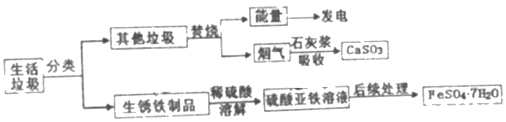
����1���������ղ����������к���SO2���к�����
����2��FeSO4���ױ������е�O2����
�ش��������⣺
��1��������ֱ���ŷţ�����ʱ�ڿ����з�����Ӧ���γ�_____ ����һ �ִ����� Ⱦ����
��2���ܽⲽ���з�����������ѧ��Ӧ�ǣ�
���� ����Fe+H2SO4 �T FeSO4 +H2�� ��Fe+ Fe2��SO4 ��3 �T3 FeSO4
a����д���ٵĻ�ѧ��Ӧ����ʽ_____��
b����Ӧ Fe+ Fe2��SO4 ��3 �T3 FeSO4�Ļ�����Ӧ������_____��
c���ܽ�ʱ�ܹ۲쵽�������й����ܽ⡢��Һ��ɫ�ı��_____��
d�������������Ʒ�к���160Kg��Fe2O3��56Kg��Fe�����������е���Ԫ�ض���ת����FeSO47H2O����Է�������Ϊ278������õ�FeSO47H2O��������_____kg��
��3���������������ٽ�����FeSO4��Һ�ڵ��������������ܼ�Ũ������ȴ�ᾧ�����˵õ�FeSO47H2O���壻����������ˮϴ��2��3���˳���FeSO47H2O���塣���е�����������_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�������ֽⷴӦ��Ϊˮ�ⷴӦ�����磺Al2S3+6H2O��2Al��OH��3��+3H2S�������������۵㣬����˵���в���ȷ���ǣ�������
A. NaF��ˮ�������NaOH��HF
B. CaO2��ˮ�������Ca��OH��2��H2O2
C. PCl3��ˮ�����֮һ��PH3
D. Mg3N2ˮ�������Mg��OH��2��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ijͬѧ��CO2����ͨ��NaOH��Һ��ͨ��һ��ʱ�����Һ�����ʵijɷ���4�ֿ������������CO2��ˮ�е��ܽ⣩���뽫������������ʵĻ�ѧʽ���������
��� | �� | �� | �� | �� |
���� | _____ | _____ | _____ | _____ |
��2����֪����Na2CO3��Һ�е���ϡ����ʱ���ȷ�����Ӧ��Na2CO3+HCl��NaHCO3+NaCl����Na2CO3��Ӧ��ȫ��������ϡ���ᣬ������Ӧ��NaHCO3+HCl��NaCl+H2O+CO2������ͬѧ��ڣ�1����������Һ����μ��뺬HCl��������Ϊ3.65%�����ᣬ��������������������CO2������������״���£��Ĺ�ϵ��ͼ��ʾ�����ͬѧ��NaOH��Һ��ͨ��CO2����Һ�����ʵĻ�ѧʽ�������ֱ�Ϊ_____��_____��
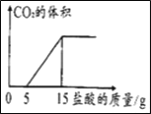
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����Χ�ơ�����кͷ�Ӧ������ѧ���ֳ�����С�鿪չ̽��������������һ���������ʵ��̽����
����ʾʵ�顿��һ����ϡ������뵽ʢ����������Һ��С�ձ��С��÷�Ӧ�Ļ�ѧ����ʽ��_____________��
���������ϡ�CaC12 ��Һ������
��������⡿ʵ����δ�۲쵽����������ͬѧ���������ʣ���Ӧ����Һ�����ʵijɷ���ʲô��
����������衿������ʣ�����ͬѧ�������£�
����I��ֻ��CaC12 ����II����__________
����III����CaC12��Ca(OH)2 ����IV����CaCl2��HCl��Ca(OH)2
����ͬѧ�����ϲ���������ɣ���Ϊ����IV����������������_________________��
��ʵ��̽����Ϊ����֤������룬��С���������������������̽����
ʵ�鷽�� | �μ���ɫʯ����Һ | ͨ��CO2 | �μ�Na2CO3��Һ |
ʵ����� |
|
|
|
ʵ������ | ____________ | __________ | ������ɫ���� |
ʵ����� | ��Һ�к���Ca(OH)2 | ��Һ�к���Ca(OH)2 | ��Һ�к���Ca(OH)2 |
���ó����ۡ�ͨ��̽����ȫ��ͬѧһ��ȷ������III����ȷ�ġ�
�����۷�˼����1������ͬѧ��Ϊ�μ�Na2CO3��Һ������ɫ������������֤����Һ��һ������Ca(OH)2�������������˵��ԭ��____________��
��2���ڷ�����Ӧ��������Һ�����ʵijɷ�ʱ�����˿����������⣮����Ҫ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��˾������������ѩ���ijɷ�����ˮCaCl2���������Ȼ��ƣ�Ϊ�ⶨ��ѩ�����Ȼ��Ƶĺ�������ѧ��ȤС���ͬѧ��ȡ����Ʒ12g����ˮ����ܽ⣬�õ���Һ50g��Ȼ��ȡһ������������̼������Һ100gƽ������μ��룬�����ʵ�����ݼ���������������ݲ������йؼ��㡣
������ | 1 | 2 | 3 | 4 | 5 |
����̼������Һ������/g | 20 | 20 | 20 | 20 | 20 |
���ɳ���������/g | 2.5 | x | 7.5 | 10 | 10 |
��1���ϱ���x����ֵΪ_____����_____�μ����̼�������Ȼ���ǡ����ȫ��Ӧ��
��2����Ʒ���Ȼ��Ƶ����������Ƕ���_____��
��3��ǡ����ȫ��Ӧʱ���ˣ����ò�������Һ���������������Ƕ���_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com