
向t ℃时饱和的Na2CO3溶液中加入n g无水Na2CO3,会析出m g Na2CO3·10H2O,则(m-n)的值为( )
A.饱和溶液失去水的质量 B.饱和溶液失去溶质的质量
C.饱和溶液失去水和溶质的质量之和 D.其数值为0,即溶液质量不变
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
今年3.11日本强烈地震引发核泄漏后,在我区出现一股抢购食盐的不良之风。其实我国食盐来源广泛 、蕴藏丰富,因此抢购食盐是完全没有必要的。已知氯化钠中氯元素在元
、蕴藏丰富,因此抢购食盐是完全没有必要的。已知氯化钠中氯元素在元 素周期表中的某些信息如图所示,下列说法错误的是:
素周期表中的某些信息如图所示,下列说法错误的是:
A. 氯元素原子在化学反应中容易得到电子,形成阴离子
B. 氯元素的核电荷数为17
C. 氯元素的相 对原子质量为35.45
对原子质量为35.45
D. 氯元素原子核外有2个电子层,最外层有7个电子
查看答案和解析>>
科目:初中化学 来源: 题型:
下列有关溶液性质的说法中错误的是( )
A.溶液一定是均一的、稳定的
B.溶液一定是无色透明的
C.食盐水能导电是因为食盐水中含有较多自由移动的离子
D.消除路面上的积雪可以撒些盐,使冰雪较快融化
查看答案和解析>>
科目:初中化学 来源: 题型:
 以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
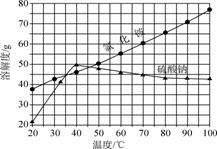
氯化铵和硫酸钠的溶解度随温度变化如下图所示。回答下列问题:(提示:氯化铵受热分
解生成氨气和氯化氢气体)
(1)实验室进行蒸发浓缩用到的主要 仪器有________、烧杯、玻璃棒、酒精灯等。
仪器有________、烧杯、玻璃棒、酒精灯等。
(2)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为____________。
(3)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列选项中括号内物质为杂质,右边为除杂试剂,其中不合理的是( )
A、氯化钠固体(碳酸钙) 水 B、氧气(水蒸气) 浓硫酸
C、硫酸亚铁溶液(硫酸铜) 铁粉 D、一氧化碳(二氧化碳) 灼热的氧化铜
查看答案和解析>>
科目:初中化学 来源: 题型:
小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:
【提出问题】猜想Ⅰ:铜与浓硫酸不能反应;
猜想Ⅱ:铜与浓硫酸能反应,且可能生成氢气。
【实验探究】实验Ⅰ:在一支试管中加入一小片铜,再加 入少量的浓硫酸,放置一段时间,试管中无现象;
入少量的浓硫酸,放置一段时间,试管中无现象;
实验Ⅱ:再给上述试管加热,试管中产生有刺激性气味的气体,将反应后的溶液小心地注入到盛有少量水的烧杯中,溶液呈现出明显的蓝色。
【分析猜想】(1)溶液呈蓝色,说明生成了 ____________
(2)根据实验现象及已有的知识推断,产生的气体不可能是氢气,很可能是一种含硫元素的气体。
【查阅资料】(1)常见的含硫元素的气体有二氧化硫和硫化氢。
(2 )二氧化硫和二氧化碳相似,都能和氢氧化钠等碱溶液反应生成盐和水。
)二氧化硫和二氧化碳相似,都能和氢氧化钠等碱溶液反应生成盐和水。
(3)二氧化硫能使品红溶液褪色,加热,又能恢复原来的红色。硫化氢不能使品红溶液褪色。
(4)二氧化硫和硫化氢均有毒。
【实验探究】为了检验产生的有刺激性气味的气体的成分,小红和她的同学进一步实验:将产生的气体通入品红溶液中,品红溶液褪色,加热,溶液又恢复了红色。
【实验结论】(1)在常温下,铜与浓硫酸不能反应。
(2)在加热条件下铜与浓硫酸反应产生的气体是____,此反应还生成了水,请写出该反应的化学方程式____________;
(3)浓硫酸与铜加热时能反应,而稀硫酸与铜即使加热也不能反应,由此说明:物质的化学性质除了与物质本身的性质有关外,还可能与溶液中溶质的____有关。
【拓展延伸】为了防止污染空气,小红和她的同学采用氢氧化钠溶液来吸收多余的气体,请写出该反应的化学方程式____________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
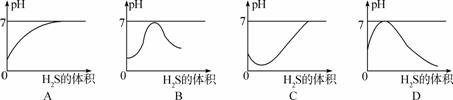
二 氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H2SO3 )。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H2S + H2SO3 === 3S↓ + 3H2O。则下图中溶液的pH随通入硫化氢的体积的变化曲线示意图正确的是 ( )
氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H2SO3 )。硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:2H2S + H2SO3 === 3S↓ + 3H2O。则下图中溶液的pH随通入硫化氢的体积的变化曲线示意图正确的是 ( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com